こんにちは。 ミドリケムです。
本日は求核性と塩基性の違いについて解説していきます。
なんとなく求核性は求電子試薬に攻撃して、その中でもプロトンを奪っているのが塩基というイメージがありますよね? 私が今まで書いてきた記事もそんな感じでしたし。
そのイメージは半分正解で半分間違っています。
今回の記事では求核性と塩基性の違いが、
・求核性:反応の速さ(速度論)
・塩基性:生成物の安定性(熱力学)
という違いを解説していきます。
求核性と塩基性の定義
結論からいうと、
求核性…電子不足な原子(主に炭素)に電子対を与える性質
塩基性…プロトン(H⁺)を受け取る性質
です。今回の塩基はブレンステッド・ローリーの定義で解説しています。
関連記事(酸・塩基の定義)

ほとんどの方々はこんなイメージだと思います。もちろん間違いではありません。冒頭でも言いましたが、これをアップデートすると、
求核性…どれだけ速く反応するか(反応速度論) 攻撃対象:主にC
塩基性…どれだけH⁺を取り安定な状態になるか(熱力学的) 攻撃対象:H+
と、物理化学の三大要素の二つ、反応速度論と熱力学が絡んできます(ちなみにもう一つは量子化学)。
求核性は、電子不足な原子にどれだけ速く攻撃できるか(反応速度)で決まるのに対し、塩基性は、プロトン(H⁺)を受け取った後にどれだけ安定な生成物になるか(熱力学的安定性)で決まります。
下の図で表すと、反応に必要なエネルギー(活性化エネルギー)が低い、つまり山が低い程、反応速度は速くなります。また、ゴールである生成物と原料とのエネルギー差(ギブス自由エネルギー)が大きい、つまり、ゴールがスタートよりエネルギーが低い程、熱力学的に安定となります。
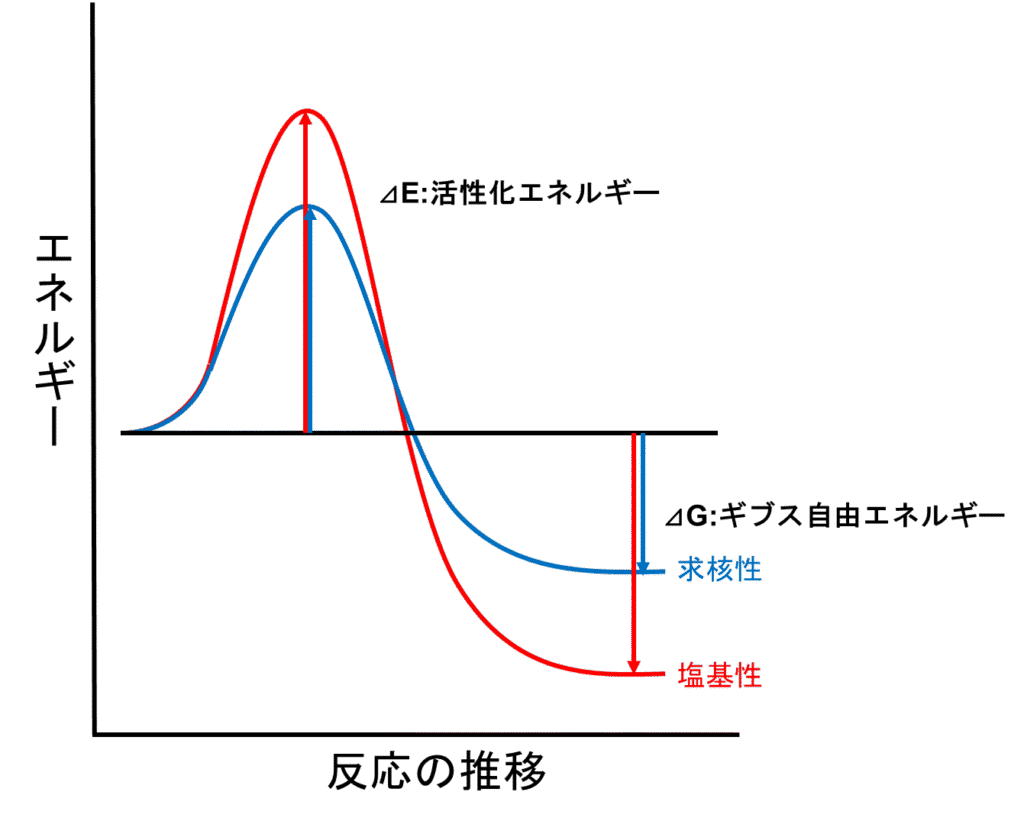
図1.求核、塩基による反応の推移とエネルギーの比較
※本来、求核性は「活性化エネルギー(速度)」、塩基性は「生成物の安定性(熱力学)」を表す概念ですが、比較しやすいよう同じエネルギー図にまとめています。反応の条件によって、エネルギー図は変わってきます。図1はわかりやすい様にあえて、スタート位置をそろえています。
では、この違いはどこで重要か?
例えばSN2反応とE2反応では:
・強い求核剤 → SN2が進みやすい
・強い塩基 → E2が進みやすい
つまり、
求核性と塩基性の違いを理解することで
「どの反応が起こるか予測できる」
ようになります。
関連記事(SN1,SN2反応)

関連記事(E1,E1cB,E2)

溶媒効果
結論からいうと、求核性は溶媒効果の影響を受け、塩基性は溶媒効果の影響をほとんど受けません。
溶媒はイオンを囲む(溶媒和)ため、求核性に影響をもたらします。特にプロトン性溶媒中では、小さい陰イオンは溶媒に強く囲まれるため反応性が低下し、大きい陰イオンほど求核性が高くなります。つまり、活性化エネルギーを大きくしてしまい、反応速度を鈍らせます。
また、SN1反応は極性溶媒、SN2反応は極性非プロトン性溶媒が良好です。
一方、塩基性は生成物の安定性(熱力学)に依存するため、溶媒の影響を比較的受けにくいです。溶媒よりも「生成物の安定性」が重要となってきます。実際、E1,E1cB,E2反応にもほとんど影響がありません。
関連記事(溶媒効果)

立体障害
これも結論からいうと、求核性は立体障害の影響を受け、塩基性は立体障害の影響をほとんど受けません。溶媒効果と同じですね。
求核試薬の攻撃対象はCです。つまり、求電子、求核試薬どちらも立体障害が大きいと求核試薬が近づけずに反応しにくく、逆に立体障害が小さいと近寄りやすくなり反応しやすいです。
塩基の攻撃対象はH+です。H+は小さいため攻撃しやすく、多少立体障害があっても問題ありません。
分極率、電子密度
原子サイズが小さいと分極率は低くなり、逆に電子密度が高いため、求核性は低いが塩基性は大きくなる傾向があります。
逆に、原子サイズが大きいほど分極率が高くなり、逆に電子密度が低いため、求核性が大きいが塩基性は低くなる傾向があります。
ハロゲンで例えると、F–は塩基性としては良好であるが求核性としては低いです。逆にI–は塩基性は低いですが、求核性は良好です。
これはHSAB則が関わっており、詳しくは以下の関連記事で記載しています。
関連記事(HSAB則)

まとめ(具体例)
・求核性:反応速度(活性化エネルギー)
・塩基性:安定性(生成物のエネルギー)
両者は似ているが本質的に異なる
表にまとめると、以下の通りです。
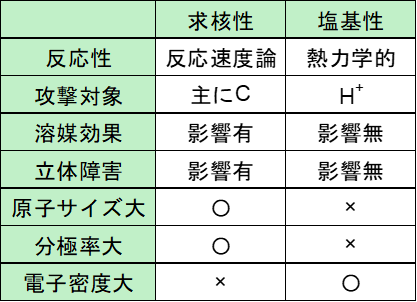
表1.求核性、塩基性の違い
また、具体例は以下の通りです。

表1.試薬による求核性、塩基性の違い
関連記事(Grignard試薬)
本日のブログはここまで。最後まで読んで頂きありがとうございました。


コメント