こんにちは。 ミドリケムです。
本日はSN1、SN2、E1、E2反応の総まとめを書いていきます。
SN1、SN2、E1、E2反応は以前にも記事として書いていますが、今回はどういう条件ならどの反応が優位なのか見分け方、反応の違いをもう少し詳しく解説していきます。
今回の記事で
・SN1、SN2、E1、E2反応の違い
・どの反応が起こるかの判断方法
・よくある間違い
が詳しく理解できます。
今回は見分け方が主なテーマなので、各反応の詳しい特徴については以下の記事をご覧ください。
関連記事(SN1、SN2反応)

関連記事(E1、E2反応)

反応を決定づける要因は主に、
・基質(第1,2,3級)
・攻撃する試薬(求核性 or 塩基性)
・溶媒効果
が決め手となってきます。どういうことなのか詳しく解説していきます。
SN1、SN2、E1、E2反応とは?
上記の記事でも解説していますが、まずは反応のおさらいです。
SN1、SN2反応は求核置換反応、E1、E2反応は脱離反応です。そして、SN1、E1反応は脱離基が脱離しカルボカチオン中間体が形成、SN2、E2反応は求核試薬、塩基が反応すると共に脱離基が同時に脱離する、いわばカルボカチオン中間体が形成しない遷移状態が発生する反応です。
ざっくり分類すると、
SN1:置換・2段階
SN2:置換・1段階
E1:脱離・2段階
E2:脱離・1段階
となります。
反応機構で解説すると以下の通りです。
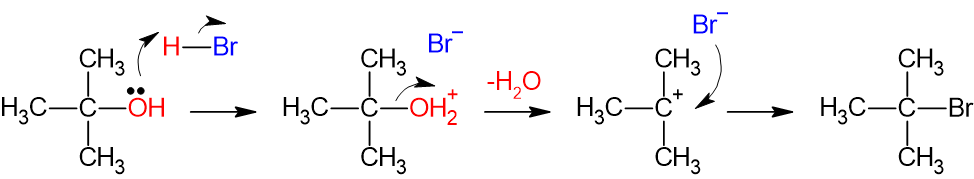
図1.SN1反応機構

図2.SN2反応機構

図3.E1反応機構

図4.E2反応機構
3つの反応の判断基準
冒頭でも言いましたが、以下の要素により、どの反応が進行するのか判断できます。
・基質(第1,2,3級)
・攻撃する試薬(求核性 or 塩基性)
・溶媒効果
ちなみに、脱離基も反応に影響していますが、脱離基は全ての反応において脱離後、溶媒効果等(主に極性溶媒)により安定していれば反応は優位に進みます。今回のSN1、SN2、E1、E2反応の区別には影響しませんので、省略します。
求核性、塩基性、溶媒効果については以下の記事に詳しく解説しています。
関連記事(求核性 or 塩基性)

関連記事(HSAB則)

関連記事(溶媒効果)

・基質(第1,2,3級)
…第1級基質だとカルボカチオンが安定しづらく、背面攻撃しやすい→SN2、E2が優位
第3級基質だとカルボカチオンが安定しやすく、背面攻撃しにくい→SN1、E1が優位
第2級基質は最も重要で、条件によってSN1・SN2・E1・E2すべてが起こり得る。
・攻撃する試薬(求核性 or 塩基性)
…強求核剤→SN1、SN2が優位
…強塩基→E1、E2が優位
・溶媒効果
…脱離基の安定化(溶媒和)により極性溶媒の方が優位
プロトン性溶媒…溶媒和によりカルボカチオンが安定化するが、同時に求核剤を強く溶媒和
するため、SN2反応を抑制する
→SN1、E1が優位
非プロトン性溶媒…カルボカチオンが生成しにくいが、攻撃試薬の邪魔をしない
→SN2、E2が優位
フローチャート
上記の3つの要素をフローチャートにまとめると、以下の通りです。
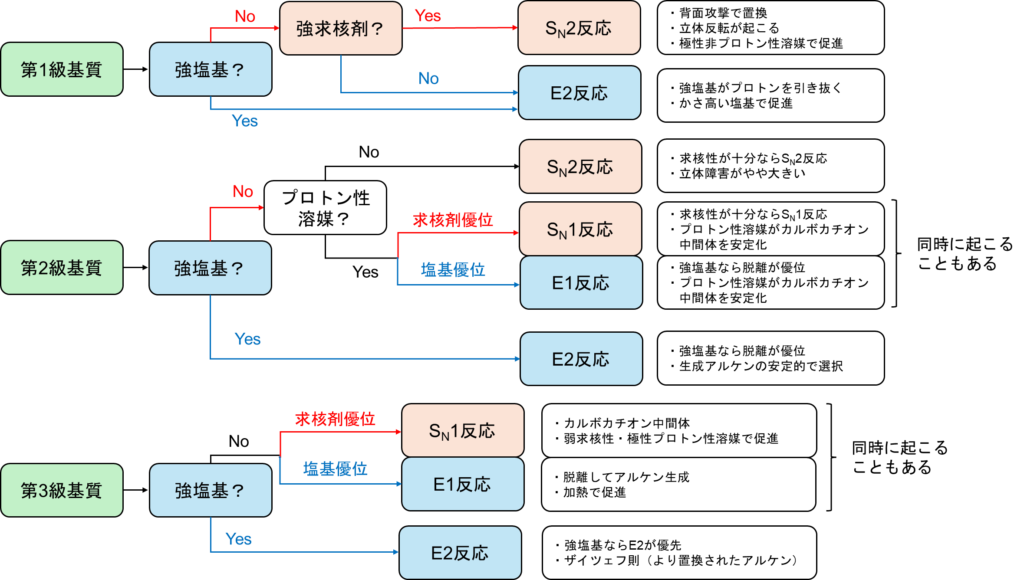
図5.SN1,SN2,E1,E2反応のフローチャート
保険をかけるようなことを言いますが、このフローチャートはあくまで一例であり、反応を保障するものではありません。基質の共鳴構造や反応条件等によっては変わってきます。
少し難しいようですが、それが化学の面白い所でもあります。
よくあるミス
・強塩基=SN2ではない
強塩基だからといってSN2になるとは限りません。むしろ強塩基はプロトンを引き抜きやすいため、
E2反応を起こしやすいです。
・求核性と塩基性は同じではない
求核性と塩基性は似ているが異なる性質です。求核性は炭素への攻撃の速さを表し、塩基性はプロトンを引き抜く強さを表します。
中にはGrignard試薬やOH–など、両方の性質を持つものもあります。
・プロトン性溶媒=SN1とは限らない
プロトン性溶媒では求核剤が溶媒和されるため、SN2反応は起こりにくくなります。しかし、必ずしもSN1になるわけではなく、条件によってはE2反応が優先します。
多くの誤解は「基質」「求核性」「塩基性」「溶媒」の違いを混同してしまうことから生じます。SN1、SN2、E1、E2は暗記ではなく、「基質」「求核性、塩基性」「溶媒効果」の3つから論理的に判断することが重要です。
具体例
次の各反応はいずれの反応が起こり、どのような生成物ができるか予測せよ。
(a)
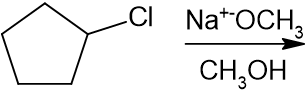
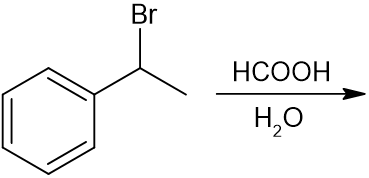
(b)
(c)
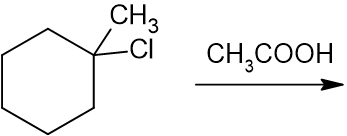
わかりましたか?答えは以下の通りです。
(a)
基質は第二級であり、強塩基を使用しています。つまり、フローチャートを見ると、答えはE2反応です。
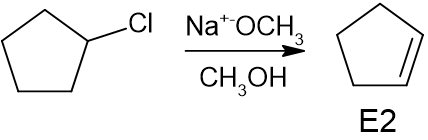
(b)
基質は第二級であり、強塩基ではありません。溶媒はプロトン性溶媒であり、ギ酸は弱塩基性でもありません(むしろ弱酸)。よって、答えはSN1反応ですが、副生成物として、E1反応も起こります。
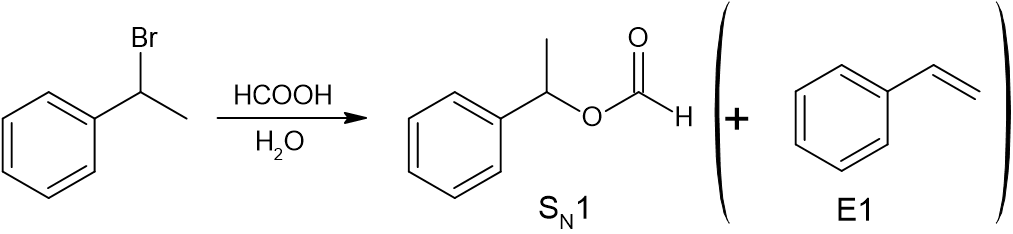
(c)
基質は第三級であり、酢酸は塩基性ではありません(むしろ弱酸)。よって、答えはSN1反応です。
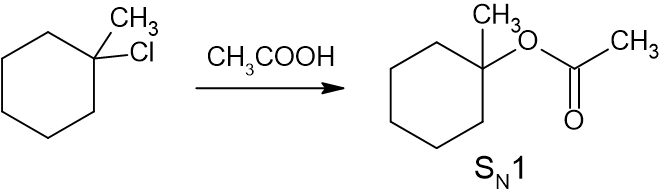
まとめ
~SN1,SN2,E1,E2反応~
・SN1、SN2反応は求核置換反応
・E1、E2反応は脱離反応
・SN1、E1反応は脱離基が脱離しカルボカチオン中間体が形成
・SN2、E2反応はカルボカチオン中間体が形成しない遷移状態が発生する反応
~反応の判断基準~
・基質(第1,2,3級)
・攻撃する試薬(求核性 or 塩基性)
・溶媒効果
参考文献「マクマリー有機化学(上)」J. McMurry 著
本日のブログはここまで。 最後まで読んで頂きありがとうございました。

コメント