こんにちは。 ミドリケムです。
本日は芳香族の置換基によって、芳香族求電子置換反応がどう影響するのか解説していきます。
芳香族求電子置換反応はルイス酸により基質をカチオン化した後、芳香族が求核攻撃して基質が置換する反応です。
しかし、芳香族はベンゼンだけではありません。トルエン、ハロゲン化ベンゼン、ベンズアルデヒド…といった様に既に置換基が導入されているものもあります。
これらの存在が芳香族求電子置換反応に影響してきます。どの様に影響してくるのか解説していきます。
本記事では主に
・置換基の誘起効果、共鳴効果
・オルト、メタ、パラ位の配向性
について解説していきます。
関連記事(芳香族求電子置換反応)
今回の記事は主にニトロ化を例に解説しますので、その項目を重点的にお読み下さい。
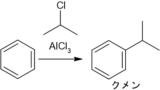
芳香環の活性化と不活性化
芳香族求電子置換反応は芳香環のπ電子が求核攻撃をして反応を始めます。つまり、芳香環に電子を富んだ置換基だと反応が活性化し、逆に電子が不足する置換基だと反応が不活性化します。前者はカルボカチオン中間体が安定化して活性化エネルギーを低めますが、後者はカルボカチオン中間体が不安定化して活性化エネルギーを高めます。
置換基による電子の吸引や供与は主に誘起効果と共鳴効果が関係してきます。それにより、置換基のオルト、メタ、パラ配向性も関係してきます。先に以下の表に結論をまとめました。

表1.置換基による芳香族求電子置換反応の反応性
上記の表の通り、誘起効果はアルキル基であるーCH3のみです。他は吸引性です(電気陰性度C>I>Br>Cl>N>O>F)。しかし、共鳴効果によっては供与性となります。ここで気をつけてほしいのはハロゲンです。有機化学の世界では基本的には誘起効果より共鳴効果の方が優先しますが、ハロゲンのみ誘起効果が優先します。
先に結論の表をまとめましたが、よくわからないかもですので、詳しく解説していきます。
関連記事(共鳴)

関連記事(Huckel(ヒュッケル)則)

トルエンの配向性
まずは表の一番上のーCH3、例としてトルエンのニトロ化で解説していきます。
芳香環に正電荷ができると、それを打ち消し合うように共鳴します。この時、オルト、パラ配向性は電子供与性基であるメチル基と結合した炭素がカルボカチオン化します。そのため、メタ位よりは安定化し、オルト、パラ位中間体の方がエネルギー順位が低く安定します。
よって、トルエンはオルト、パラ位にニトロ基が置換します。
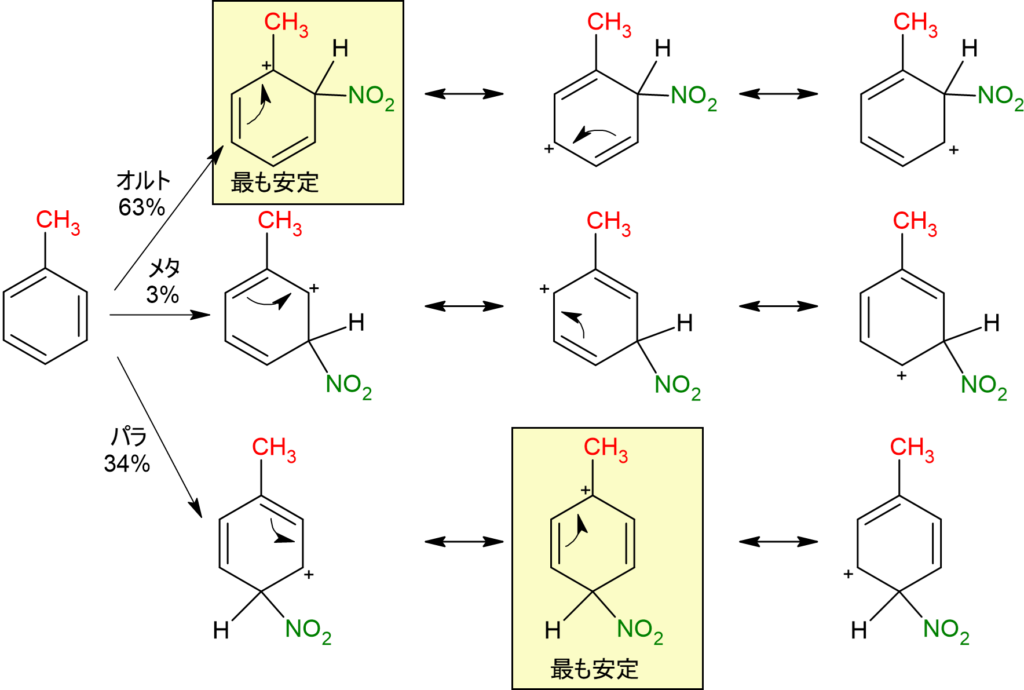
図1.トルエンのニトロ化
フェノールの配向性
次に、表の二番目のーOH, ーNH2、例としてフェノールのニトロ化で解説していきます。
トルエンと違い、フェノールの置換基ーOHは弱い電子吸引性誘起効果に打ち勝つような強い電子供与性共鳴効果をもっています。この時、オルト、パラ中間体がより多くの共鳴構造をもち、特に酸素からの電子対の供与によって正電荷が安定化された共鳴構造が存在します。メタ中間体はそのような安定化をもちません。そのため、メタ位よりは安定化し、オルト、パラ位中間体の方がエネルギー順位が低く安定します。
よって、フェノールはオルト、パラ位にニトロ基が置換します。アニリンも同様です。
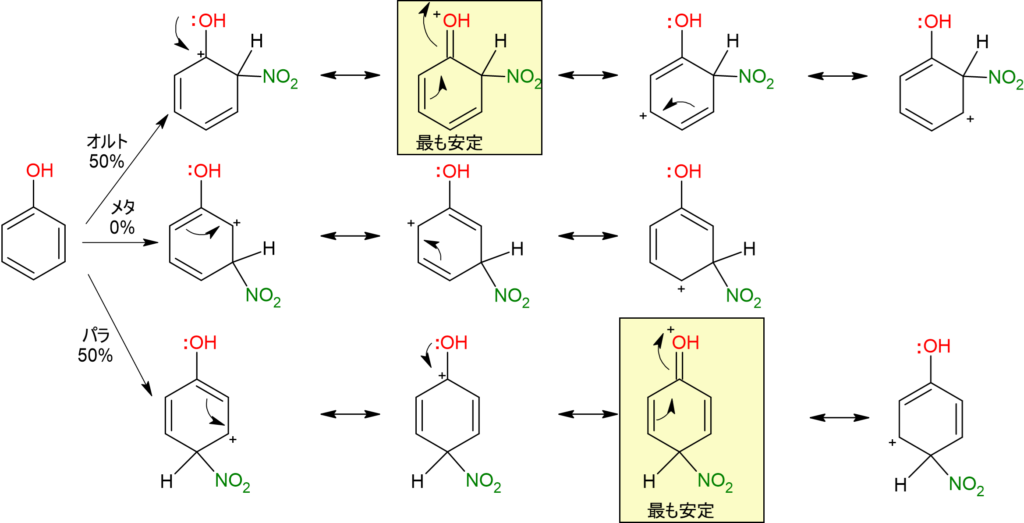
図2.フェノールのニトロ化
クロロベンゼンの配向性
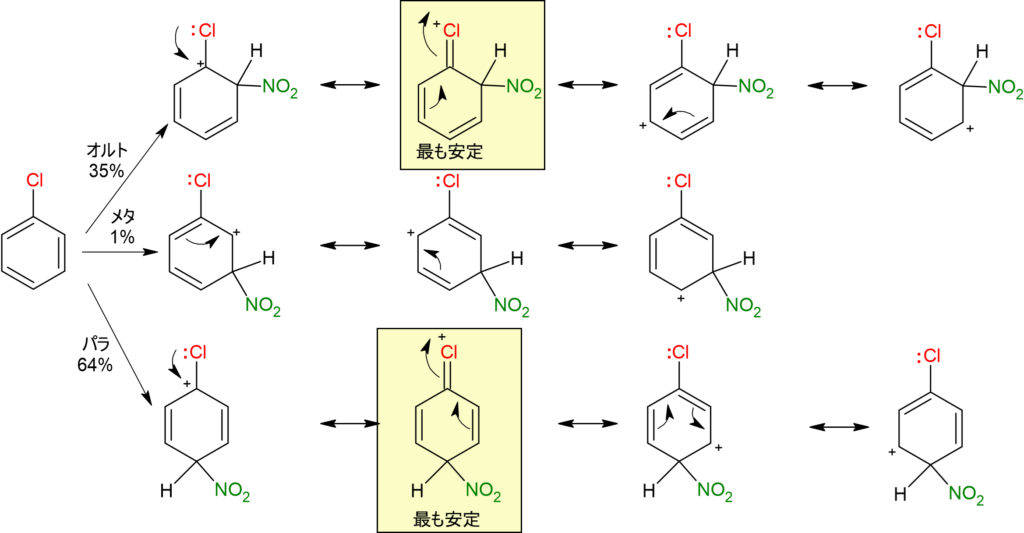
次に、表の三番目のハロゲンについて解説していきます。ハロゲンは先程も言いましたが、強い電子吸引性誘起効果が弱い電子供与共鳴効果に打ち勝つため、不活性基です。弱いとはいえ、その電子供与性共鳴効果はオルト、パラ位に配向しています。例として、クロロベンゼンで解説していきいます。
解説といいましたが、結局のところ、先程のフェノールと変わりありません。よって、ハロゲン化ベンゼンもオルト、パラ位に配向します。
しかし、フェノール、アニリンは電子供与性共鳴効果が強いため活性化しますが、ハロゲン化ベンゼンは電子吸引性誘起効果が強いため不活性化します。
ベンズアルデヒドの配向性
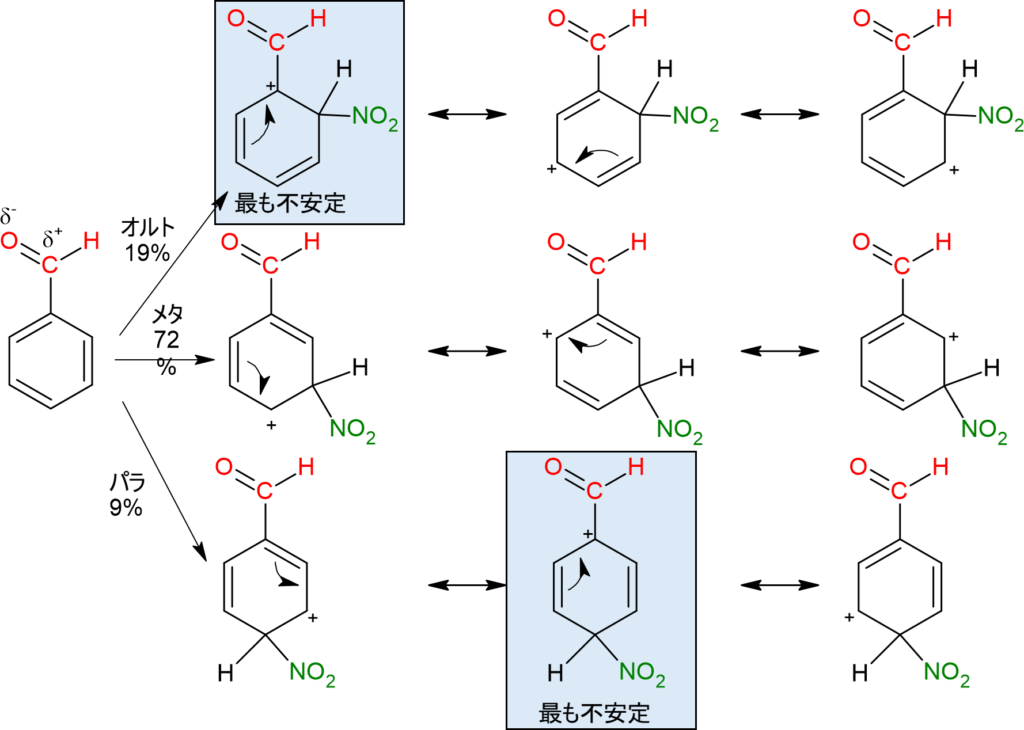
最後に表の一番下の項目、例としてベンズアルデヒドについて解説していきます。
これは誘起、共鳴効果共に電子吸引性基です。そのため不活性です。一応反応機構を見ると、オルト、パラ位の場合、置換基の付け根の炭素にカルボカチオン中間体が存在します。置換基は電子吸引性であるため、不安定です。そのため、オルト、パラ位中間体の方がエネルギー順位が高く不安定します。
よって、ベンズアルデヒドはメタ位にニトロ基がつきますが、基本的には不活性です。
まとめ
もう一度先程の表です。これが今回言いたかったことです。

参考文献「マクマリー有機化学(中)」J. McMurry 著
今回は二置換体ベンゼンについて解説しましたが、三置換体のことについても詳しく記載しています。もう少し芳香族の反応について詳しく知りたい方はオススメです。
本日のブログはここまで!! 最後まで読んで頂きありがとうございました!!
コメント