こんにちは。 ミドリケムです。
本日はHSAB則について解説していきます。
「求核性の強さって何で決まるの?」
「なぜヨウ化物イオンは強い求核剤なのか?」
こうした疑問は、HSAB則(硬い・柔らかいの概念)で説明できます。
この記事では、
・HSAB則とは何か
・硬い酸・柔らかい酸の違い
・求核性との関係
を、直感的にわかりやすく解説します。
関連記事(酸・塩基)

HSAB則とは?
HSABはHard Soft Acid Baseの頭文字をとったものであり、要は硬い酸・塩基、柔らかい酸・塩基のことです。ここでの硬い、柔らかいは以下の定義の通りです。
硬い…小さい・電荷密度高い(イメージとしては小さくてカチカチ)
軟らかい…大きい・分極しやすい(イメージとしては大きくてふにゃふにゃ)
そして、結論からいうと、硬いもの同士、軟らかいもの同士は相性が良いです。これは「硬い酸は硬い塩基と、柔らかい酸は柔らかい塩基と優先的に結合する」という経験則です。
この考え方がHSAB則であり、求核性の違いも説明できます。
イメージしやすくすると、以下の図の通りとなります。

図1.硬さ・軟らかさの異なる酸・塩基の対の結合
図からわかる通り、硬い酸・塩基はそれぞれの結合間距離が長く、逆に軟らかい酸・塩基は結合間距離が短いです。
つまり、硬い酸と硬い塩基の結合は、主に静電的な相互作用(イオン結合)で安定化されます。
一方、柔らかい酸と柔らかい塩基の結合は、軌道の重なり(共有結合的相互作用)によって安定化されます。
この違いにより、この違いにより、「硬い同士」「柔らかい同士」が安定になります。
関連記事(イオン結合、共有結合)

また、HSAB則の具体例として、以下の表にまとめました。

表1.HSAB則の具体例
参考文献「ベーシックマスター 無機化学」増田 秀樹、長嶋 雲兵 共編
F–とI–の違い
ここで、F–とI–の違いを解説していきます。
塩基性
F–は硬い塩基なのに対し、I–は軟らかい塩基です。また、プロトンH+は硬い酸です。そのため、同じ硬いもの通しのF–はH+と相性が良いですが、I–との相性はいまいちです。そのため、前者はブレンステッド・ローリーの定義では塩基性を示しますが、後者は塩基性を示しません。
ちなみに、フッ化水素HFはイオン結合ではなく共有結合ですが、他のハロゲン化水素と違い水中でもあまり共有結合を切り離しません。結合力もHF>HCl>HBr>HIです。それどころか、水素結合により、分子間結合もするため、ハロゲン化水素の中でも唯一の弱酸です。
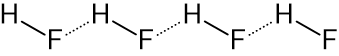
図2.フッ化水素の分子間結合(水素結合)
求核性
溶媒がプロトン性溶媒である時、F–は小さく電子密度が高いためプロトン性溶媒にガチガチに拘束されてしまい求核性をあまり示しません。逆に、I–は大きく広く分極しているためプロトン性溶媒にあまり拘束されず、求核性が良好です。つまり、求核性はI–>Br–>Cl–>F–です。以下にプロトン性溶媒中のイオンの拘束について図示します。

図3.プロトン性溶媒によるハロゲンの拘束(R=Hの時は水)
プロトン性溶媒では、小さいイオンほど強く溶媒和される
逆に、溶媒が非プロトン性溶媒である時、F–は電子密度が高いため本来の塩基性がそのまま求核性として示しやすく、逆にI–はあまり求核性が変わりません。つまり、求核性はI–<Br–<Cl–<F–です。
溶媒や反応条件にもよるためきっちりと逆転が起こるかは難しいですが、重要なのは小さいイオンほど強く溶媒和されて不利になるということです。
言い換えると、硬いイオンは溶媒和されやすく、柔らかいイオンは溶媒和されにくいです。やはり、求核性は溶媒効果が影響されにくいI–が良好ですね。
関連記事(求核性、塩基性)

関連記事(溶媒効果)

まとめ
・HSABはHard Soft Acid Baseの頭文字をとったもの
硬い…小さい・電荷密度高い(イメージとしては小さくてカチカチ)
軟らかい…大きい・分極しやすい(イメージとしては大きくてふにゃふにゃ)
・硬いもの同士、軟らかいもの同士が相性が良い(前者は静電的に安定(イオン結合)、後者は軌道の重なりで安定(共有結合))
・硬い塩基はブレンステッド・ローリーの定義の塩基、柔らかい塩基は求核性を示しやすい(溶媒効果によって逆転も起こる)
本日のブログはここまで!!最後まで読んで頂きありがとうございました!!



コメント