こんにちは。 ミドリケムです。
本日は芳香族がなぜ安定化か解説していきたいと思います。
ベンゼンは二重結合を3個持っていますが、ビニル基みたいにπ結合を開裂して重合するのか? 答えはNoです。
ベンゼンを含んだ芳香族はビニル基の様な二重結合とはちょっと違った性質を持っています。詳しく解説していきます。
当記事では主に
・共鳴安定化(原子価結合法)
・Huckel則(分子軌道法)
・ピリジンとピロール、ナフタレンとアズレンの違い
について詳しく解説していきます。
共鳴安定化(原子価結合法)
この内容は以下の記事でも解説しましたが、もう一度おさらいします。
関連記事(共鳴)

ベンゼンの6つの炭素は全てsp2混成軌道でしたね。その混成軌道は他の炭素、水素とσ結合します。そして、混成されなかったp軌道上の電子をπ電子と呼び、そのp軌道同士で軌道が広がりπ電子が飛び回ります。これを共鳴と呼びましたね。

図1.ベンゼンの共鳴の模式図
3つ以上の炭素上のp軌道に電子が飛び回ることを非局在化と呼びます。ベンゼンの構造式は以下の様に単結合と二重結合が交互に書かれていることが多いですが、実際はπ電子が飛び回っているため、1.5結合(こんな名称はありませんが…)というイメージが正しいです。

図2.ベンゼンの共鳴構造式
また、単結合と二重結合が交互に連なりp軌道が広がったことをπ共役系と呼びます。ベンゼンもπ共役系です。
また、p軌道が広がりπ電子が非局在化するため、π共役系を含んだ共鳴構造部分は平面構造をしています。
復讐になりましたが、以上が原子価結合法による解説です。
Huckel則(分子軌道法)
Huckel則とは?
共鳴の解説を聞くと、「環状で単結合、二重結合が交互に連なった化合物が芳香族」と思ってしまいますよね? 残念ながらそうではありません。
ベンゼンは平面構造であり芳香族です。しかし、シクロオクタテトラエンは平面構造ではなく芳香族ではありません。実際はおけ形をしており(以下の図では上手く描けませんでした…)、π電子も局在化しています。
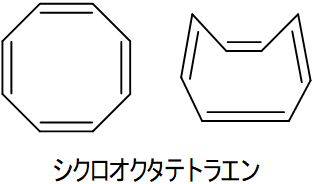
図3.シクロオクタテトラエンのおけ形構造式
原子価結合法ではよくわからないため、ここで分子軌道法で考えていきましょう。ベンゼンの六つの炭素上のp軌道を環状に組み合わせると、以下の図の通りになります。
結合性軌道に最もエネルギーの低い一つの軌道と二つの同じエネルギーの軌道、反結合性軌道に二つの同じ軌道と最もエネルギーの高い一つの軌道があります。それらを順にπ電子が対を成して電子が収容されます。
元の軌道から低いエネルギー準位で安定した軌道を結合性軌道、反対に高いエネルギー準位で不安定な軌道を反結合性軌道といいます。
結合性軌道は分子内の結合力を高め、反結合性軌道は結合力を弱めます。ベンゼンのπ電子は結合性軌道にスッポリ収まります。
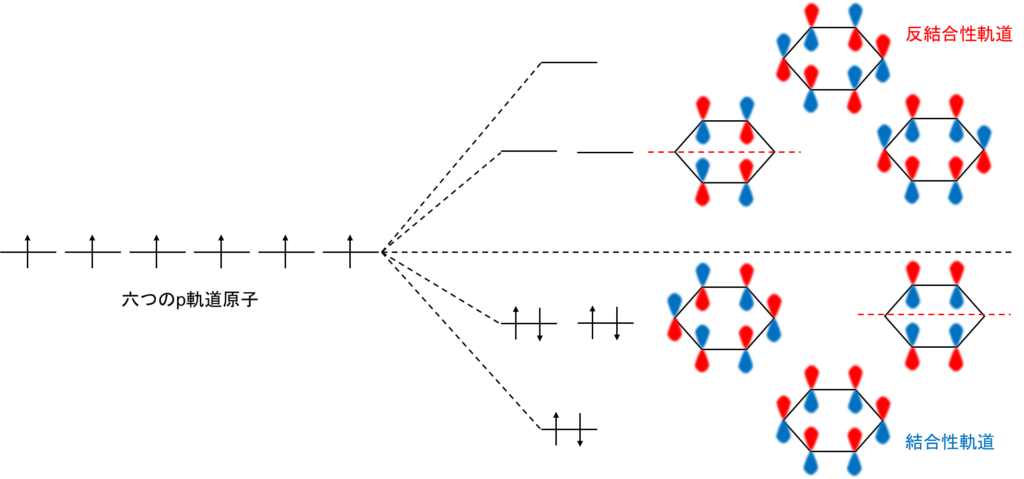
図4.ベンゼンのp軌道の分子軌道法の模式図
ベンゼンのπ電子は6つであるため3つの結合性軌道(1+2)、3つの反結合性軌道(1+2)ができましたが、炭素が増えるごとに結合性軌道、もしくは反結合性軌道がそれぞれ2つずつ増えていきます。
つまり、π電子が(4n+2)個あると、芳香族として安定化します。これをHuckel(ヒュッケル)則と言います。
ベンゼンのπ電子は6個((4×1+2)個)であるためHuckel則を満たしますが、シクロオクタテトラエンのπ電子は8個であるため、Huckel則を満たしません。よって、前者は芳香族ですが、後者は芳香族ではありません。
今回は結合性軌道、反結合性軌道について解説しましたが、非結合性軌道というものも存在します。
関連記事(超原子価結合、非結合性軌道)

参考文献「マクマリー有機化学(中)」J. McMurry 著
芳香族のことに関して詳しく記載されています。
参考文献「「量子化学」のことが一冊でまるごとわかる」齋藤勝裕 著
量子化学をメインに記載されています。量子化学視点で有機化学のことも記載されています。
Huckel則の例
Huckel則の例をいくつかご紹介します。
ピリジンとピロール
結論から言うと、ピリジンもピロールもHuckel則を満たしておりどちらも芳香族です。ではなぜこの二つを比較するのかというと、同じ窒素Nでもπ共役系に関わっている電子が違うからです。
窒素には一つの非共有電子対を持っていましたね。ピリジンの非共有電子対はsp2混成軌道に存在します。そして一つの電子はp軌道に存在し、他の5つの炭素のπ電子と軌道を広げπ共役系として非局在化します。合計6つのπ電子なのでHuckel則を満たします。
一方、ピロールの非共有電子対はp軌道に存在します。そして、他の4つの炭素のπ電子と軌道を広げπ共役系として非局在化します。こちらも、合計6つのπ電子なのでHuckel則を満たします。重要なのは、非共有電子対が非局在化していることです(というか、非局在化しているため、非共有電子対と呼ぶのも怪しいですが…)。そのため、ピリジンは塩基性を示します(酸解離定数pKa=5.25)が、ピロールはほとんど塩基性を示しません(酸解離定数pKa=0.4)。
以下に軌道図を載せておきます。
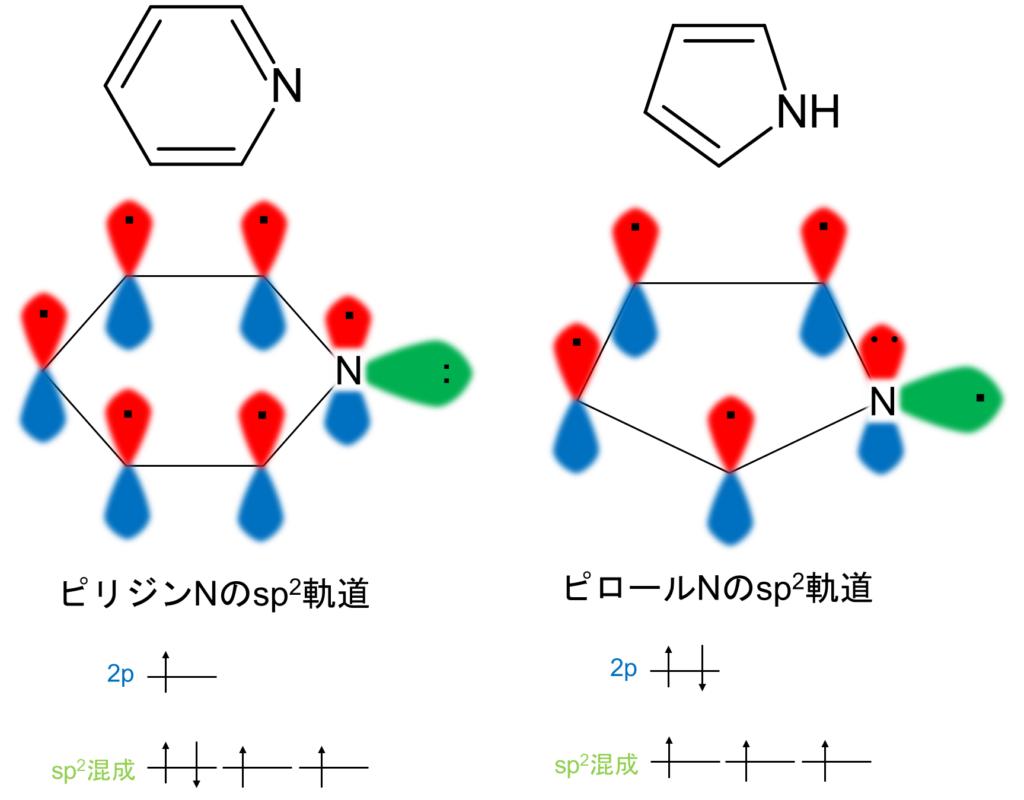
図5.ピリジンとピロールとの軌道の模式図
参考文献「マクマリー有機化学(下)」J. McMurry 著
含窒素分子(アミン、アニリン類)のことについて詳しく記載されています。
ナフタレンとアズレン
こちらも結論から言うとどちらも芳香族です。化学式もどちらもC10H8です。では何が違うのかというと、電荷の隔たりの有無です。
ナフタレンは6員環が2つ結合した構造であり、どちらも6π電子をもっているため、安定化します。
アズレンは5員環には5π電子、7員環には7π電子を持っています。そのため、安定した6π電子にするには5員環はマイナスに、7員環はプラスになる必要があります。これにより、どちらも6π電子となり安定化しますが、電荷の隔たりが無いナフタレンの方が安定です。
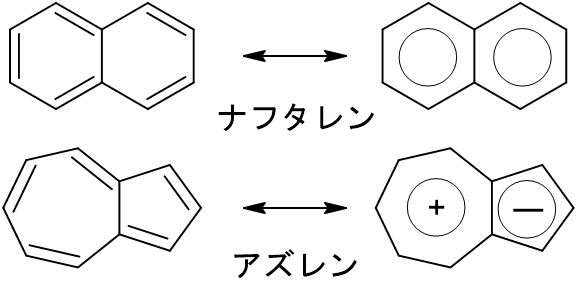
図6.ナフタレンとアズレンの共鳴構造式
π共役系が広がると…
上述のπ共役系が広がると、HOMOとLUMOの間隔(バンドギャップ)が狭くなります。つまり、電子が低エネルギーでも励起しやすくなります。主に芳香族はこのバンドギャップが低いです。
低エネルギー、特に可視光で励起状態になると色が着きます。上記のアズレンは青色です。そのため、染料、顔料は芳香族がほとんどです。
関連記事(色素)

この様に化学では原子価結合法、分子軌道法と二つの結合論で議論していくことが重要になります。電子や原子は眼では見えないためイメージしづらいかもしれませんが、これも訓練ですね。かくいう私も苦労しました。
まとめ
・共鳴…p軌道同士で軌道が広がりπ電子が飛び回り安定する現象
・Huckel則…電子が結合性軌道に収容され、π電子が(4n+2)を満たし、芳香族として安定する現象
・構造によって、非共有電子対の収容される軌道が変わり、塩基性等特性が変わる。
次回の記事ではこのπ共役系についてもう少し詳しく解説しようかと思います。そして、これにより日本人が生み出した功績、導電性ポリマーについても解説していきます。
関連記事(π共役系)

また、この様な安定している芳香族でも反応は起こります。
関連記事(芳香族求電子置換反応)
本日のブログはここまで。 最後まで読んで頂きありがとうございました。

コメント