こんにちは。 ミドリケムです。
本日は溶媒効果について解説していきます。
溶媒効果とは、溶媒がイオンや分子を安定化することで反応速度や平衡を変える現象です。
溶媒は反応を支配するといっても過言ではありません。この記事のカテゴリーは「無機化学」ですが、当然、有機化学にも影響してきます(カテゴリー選択に迷いましたが…)。
今回の記事で
・溶媒の種類
・なぜ、溶媒によって反応が決まるのか?
・有機化学での溶媒
について解説していきます。
溶媒の種類
水
まずはじめに水について解説していきます。水は誰もが知っているH2Oです。これは分子量約18g/molであり、小さな分子で本来はN2やCO2と同様、気体としか存在することができません。しかし、水は液体、ないし固体と姿を変える物質です。ではなぜ、液体、固体となるのでしょうか?
答えは水素結合です。電気陰性度はO>Hです。そのため、OはHから電子を引っ張っています。さらに、酸素上の2つの非共有電子対が電荷反発をし、水分子は折れ線の形状をします。そのため、かなり分極しており、Oが負電荷寄り、Hが正電荷寄りしています。そのため、分子間上に水素結合という弱い相互作用が生まれます。図示すると、以下の通りです。

図1.水分子同士の水素結合による相互作用
関連記事(水素結合)

上記の通り、水分子同士が凝集し合います。そのままOがHを引っこ抜き、以下の反応も起こります。
2H2O⇆H3O++OH–
もちろん、H3O+からプロトンが引っこ抜かれたり、逆にOH–がプロトンを引っこ抜いたりします。いわば、水は酸素原子によるプロトンの取り合いです。この反応は高速に行われます。水はアレニウスの定義で中性を示しますが、これは、「酸でも塩基でもない」というよりは「酸でも塩基でもある」が正しいです。酸として、塩基として平衡して反応が行われているため、中和され「中性」と名乗っているのです。
ちなみに、分極を示す指標として、誘電率があります。また、真空の誘電率で割ったものを比誘電率といいます。これらが高い程、分極されています。水の比誘電率は78.54(25℃)で溶媒の中でもかなり高いです。
ここで、水に酸や塩基を加えると以下の電離が起こります。
酸:A-H+H2O→A–+H3O+
塩基:B+H2O→B+-H+OH–
この通り、酸を加えた場合水は塩基になりH3O+の比率が多く水溶液は酸性、逆に塩基を加えた場合、水は酸になりOH–の比率が多くなり水溶液は塩基性となります。では、発生したA–、B+はどうなるのでしょうか?
答えは誘電率の高い水は+にもーにも分極されており、A–は+に分極されているHに、B+はーに分極されているOに囲まれて安定化します。これを溶媒和、特に水溶液の場合では水和といいます。
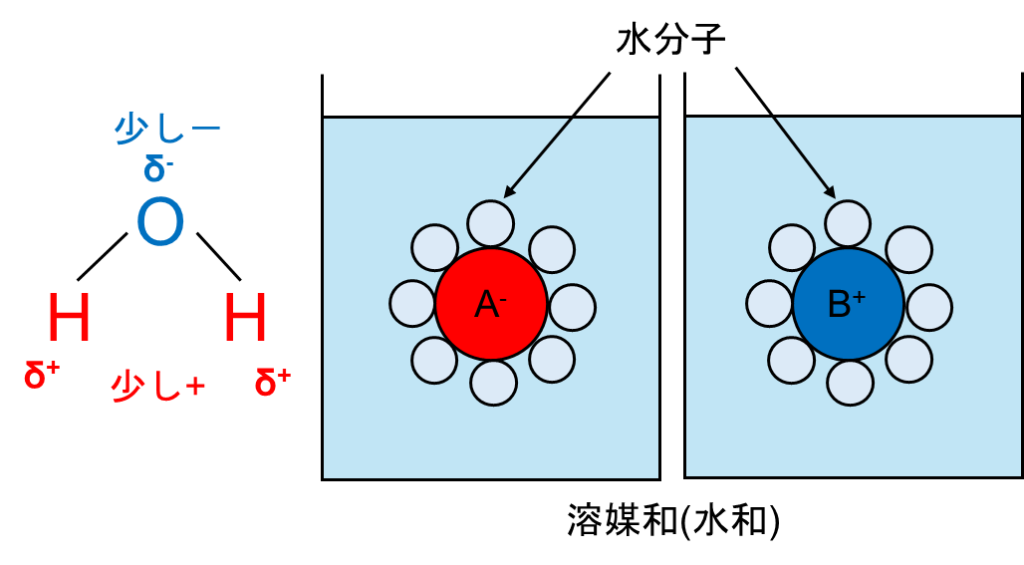
図2.溶媒和(水和)
溶媒和によりイオンは安定化され、電離が起きやすくなります。言い換えると、溶媒和によって、イオンは安定化され他の物質と反応することが難しくなります。溶媒は時によっては反応を促進したり(電離等)、逆に反応を阻害したり(イオンの安定化等)します。これは重要なので覚えておいてください。
非水溶媒(有機溶媒)
次に非水溶媒、つまり有機溶媒です。これはプロトン性溶媒、非プロトン性溶媒(極性有りor無し)にわかれます。
プロトン性溶媒
まずはプロトン性溶媒です。代表的なのはメタノール、エタノールといった低級アルコールです。これらの溶媒も水と同様、水素結合を形成したり、プロトンを放出したりします。
水素結合を形成するため、沸点も上昇します(メタンCH4(-161.5℃) メタノールCH3OH(64.7℃)、エタンC2H6(-88.5℃) エタノールC2H5OH(78.3℃))。
また、プロトンを放出して電離もします。
ROH⇆RO–+H+ (R=CH3, C2H5)
この平衡は高速に行われますが、比誘電率はメタノール32、エタノール24(25℃)と水78.54(25℃)に比べるとはるかに低くRO–、H+の濃度比率はかなり低いです。RO–を生成するには塩基を加えプロトンを引っこ抜くことで生成します。
ここで、水に酸や塩基を加えると以下の反応が起こります。
酸:A-H+ROH→×(反応が起こらない)
塩基:B+ROH→B+H+RO–
プロトン性溶媒より強い酸を加えると、その酸が電離してプロトン濃度が上がりアルコールの電離を逆に妨げて(上述の平衡では右側方向が優位)反応が起こりません。一方、塩基を加えると、上述の通り、塩基がアルコールからプロトンを引っこ抜き、塩基とプロトンが共有(配位)結合(塩基が水酸化物イオンの場合、水)し、さらにアルコキシイオンが生成します。このアルコキシイオンが他の化合物と反応、もしくは金属イオンとイオン結合を形成します。
同じプロトンを放出する溶媒でも水と大違いですね。他にもプロトン性溶媒はカルボン酸などもあります。こちらはプロトン脱離後、共鳴効果によりカルボキシアニオンが安定化するため、アルコールよりもプロトンを放出しやすい、つまり酸性度が高いです。
関連記事(共鳴)

非プロトン性溶媒
非プロトン性溶媒は以下の通りです。簡単に説明します。
・極性非プロトン性溶媒
…プロトンを放出せず、さらに水素結合をあまり示さないが、分極したN,O等が存在するため、強くイオンに溶媒和する溶媒
(例:アセトニトリル、テトラヒドロフラン(THF)、ジメチルスルホキシド(DMSO)、ジメチルスルホキシド(DMSO) etc.)
・非極性非プロトン性溶媒
…極性や誘電率が低く、イオンなどの溶解性も低いため、極性物質を溶解する能力が小さい。
(例:脂肪族・芳香族炭化水素、四塩化炭素 etc.)
参考文献「ベーシックマスター 無機化学」増田 秀樹、長嶋 雲兵 共編
有機化学での例
有機化学において溶媒効果が最も重要なのは、溶媒によって求核性の順序が逆転する点です。プロトン性溶媒と非プロトン性溶媒とではハロゲンを例とすると、求核性がプロトン性溶媒ではI–>Br–>Cl–>F–です。理由としては、F–は小さく電子密度が高いためプロトン性溶媒にガチガチに拘束されてしまい求核性をあまり示しません。逆に、I–は大きく広く分極しているためプロトン性溶媒にあまり拘束されず、求核性が良好です。

図3.プロトン性溶媒によるハロゲンの拘束(R=Hの時は水)
プロトン性溶媒では、小さいイオンほど強く溶媒和される
逆に、溶媒が非プロトン性溶媒では求核性はI–<Br–<Cl–<F–です。理由として、水素結合が無いため、電子密度が高いF–は本来の塩基性がそのまま求核性として示しやすく、逆にI–はあまり求核性が変わりません。
溶媒や反応条件にもよるためきっちりと逆転が起こるかは難しいですが、重要なのは小さいイオンほど強く溶媒和されて不利になるということです。やはり、求核性は溶媒効果が影響されにくいI–が良好ですね。
関連記事(HSAB則) ほとんど同じことを記載しています。

関連記事(求核性、塩基性)

また、プロトン性溶媒は求核性を落とす要因にもなるため、SN2反応では使用を避けた方が良いです。
関連記事(SN1、SN2反応)

まとめ
・水は比誘電率の高いプロトン性極性溶媒、水素結合により低分子でも常温常圧で液体として存在し、溶媒和(水和)により溶質を電離、条件によって酸にも塩基にもなる中性溶媒
・非水溶媒(有機溶媒)はプロトン性溶媒、非プロトン性溶媒に分類
・プロトン性溶媒は水素結合を起こしやすく、塩基との共存により、酸として働く
・非プロトン性溶媒はさらに極性非プロトン性溶媒、非極性非プロトン性溶媒に分類
・プロトン性溶媒は水素結合による阻害により求核性I–>Br–>Cl–>F–、非プロトン性溶媒では水素結合が無いため、I–<Br–<Cl–<F–
本日のブログはここまで!! 最後まで読んで頂きありがとうございました!!


コメント