こんにちは。 ミドリケムです。
本日はカルボニル化合物の構造・性質・求核反応をわかりやすく解説していきます。
本記事は
・カルボニル化合物とは?
・カルボニル化合物の還元反応
・カルボン酸からエステル化、アミド化
・酸ハロゲン化物の生成、および反応性
について解説していきます。
カルボニル化合物とは
カルボニル化合物はその名の通り、カルボニル基C=Oが存在する化合物の総称です。下図に示している通り、第1級、第2級アルコールが酸化したアルデヒド、ケトン、カルボン酸、さらにはカルボン酸から反応した酸塩化物、エステル、アミド、およびチオエステル等、様々な化合物があり、他にも存在します。
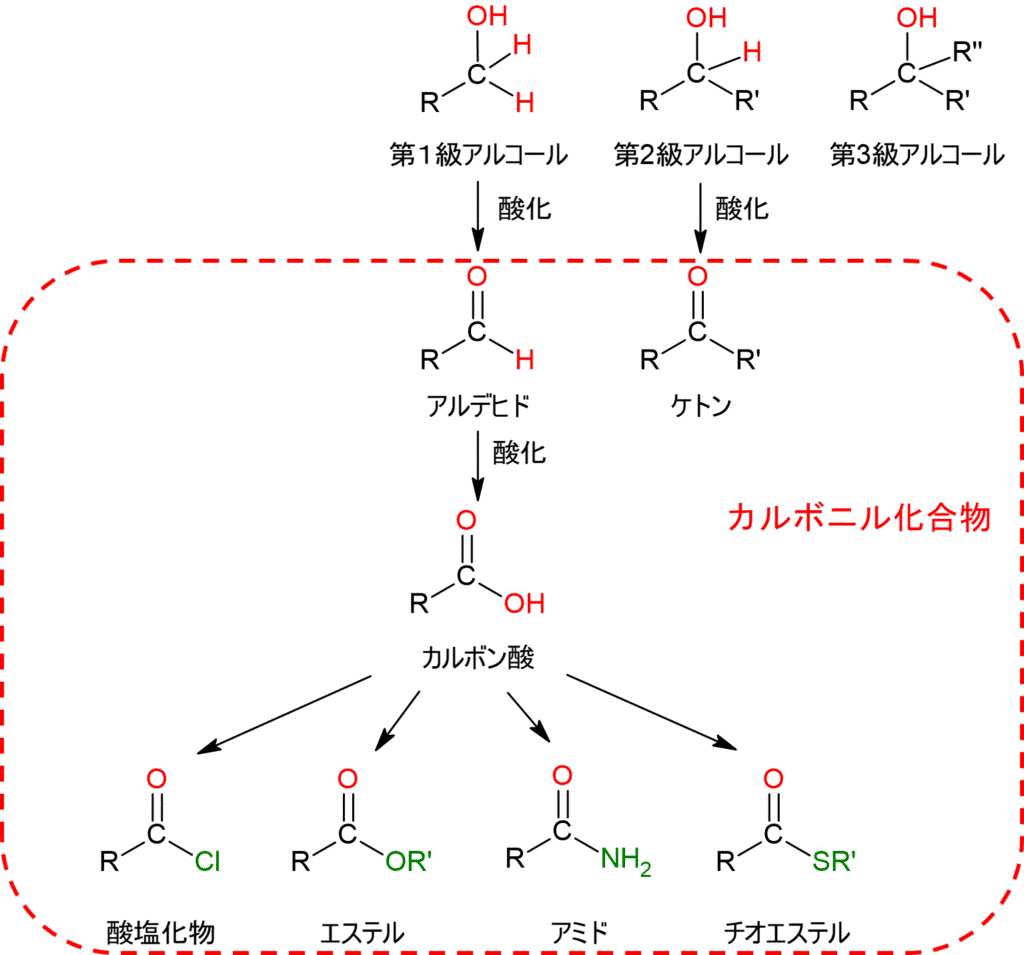
図1.カルボニル化合物の一覧
C=O結合の電子構造
C=O結合は電気陰性度C<Oのため、Cδ+、Oδ-、つまり電子がOに引っ張られています。
関連記事(電気陰性度)

他にも、C=O上のC,Oはsp2混成軌道であり、π電子がC、O上のp軌道間を飛び回ります。
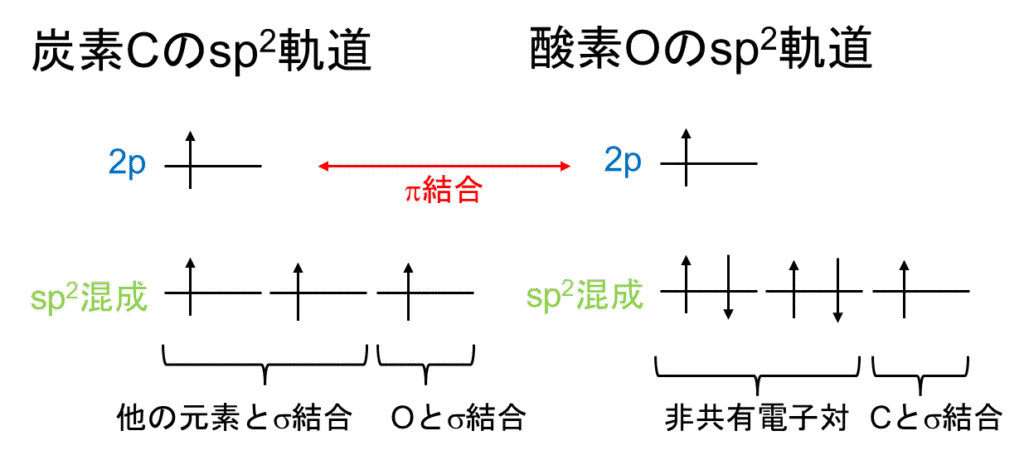
図2.炭素C、酸素Oのsp2混成軌道
関連記事(sp2混成軌道)

以上のことから、カルボニル炭素Cは正に強く分極しており、求核攻撃がされやすい、つまり求電子性を示します。逆に、カルボニル酸素Oは負に強く分極しており、求核攻撃をしやすいです。
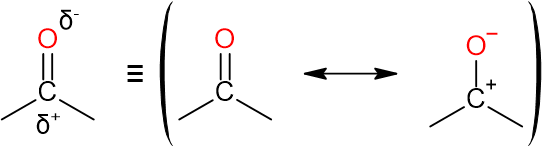
図3.カルボニル基の分極
カルボニル化合物の反応(求核付加)
還元反応
初めにGrignard試薬との反応性です。Grignard試薬は良好な求核試薬なため、求電子性のあるカルボニル炭素に求核攻撃します。すると、正四面体中間体が生成し、水で処理することでアルコールを生成します。

図4.アルデヒド、ケトンとのGrignard反応
関連記事(Grignard試薬)
もちろん、還元剤LiAlH4、NaBH4を用いることでもアルコールに変換できます(Grignard試薬も求核攻撃するので還元剤とも言えますが…)。ここで大きな違いは還元剤は水素を添加しますが、Grignard試薬は置換基(図4でいうとーR3)を導入することです。
ちなみに、還元剤LiAlH4、NaBH4は前者の方が還元力が強いです。比較すると、以下の表の通りとなります。

表1.還元剤LiAlH4、NaBH4で還元できる化合物の一覧
LiAlH4の方が還元力は強いですが、引火しやすかったりとかなり危険です。取扱はSDSを要チェックして下さい。
また、反応性としてはアルデヒド>ケトンです。理由としては、1つ目は立体障害が低いからです。2つ目としては、ケトンはアルキル基を2つ持つため電子供与性が大きく、カルボニル炭素の正電荷が緩和されます。その結果、アルデヒドに比べて求電子性が低く、反応性も低下するからです。
カルボン酸からエステル化
カルボン酸から塩酸や硫酸といった強酸を触媒として用いて脱水縮合し、エステル化する手法があります。これをFischer(フィッシャー)エステル化といいます。
反応機構としては、カルボニル酸素が酸を引っこ抜きカチオン化します。すると、カルボニル炭素は求電子性を強く示し、アルコールのヒドロキシ酸素にも攻撃され正四面体中間体を生成します。その後、プロトンが転移し、水分子として脱離しやすくなります。最後に、プロトンが脱離されることで酸触媒が再生され、エステル化されます。
しかし、この方法が多量のアルコール溶媒が必要となるため、メタノール、エタノール、プロパノール、およびブタノールといったアルコールしか使えません。また、矢印を⇆を使用しているため、可逆反応です(そのため、アルコールが多量必要となります)。
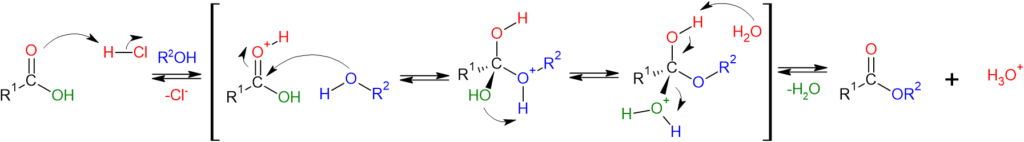
図5.Fischerエステル化
他にもカルボン酸をアルカリ処理でアニオン化した後、SN2反応によりエステル化されます。ちなみに、エステルはアルカリに弱くすぐ加水分解されるため、アルカリ処理後は余剰のアルカリを取り除く必要があります。

図6.SN2反応によるエステル化
関連記事(SN2反応)

カルボン酸からアミド化
カルボン酸とアミンからアミド化することもできますが、基本的にはこの2つだけではアミド化は起こりません。カルボン酸は酸、アミンは塩基であるため、アミンがカルボン酸からプロトンを奪って反応は終わりです。
そこで、カルボン酸のーOH基を非酸性のより優れた脱離基に変える必要があります。ここで登場するのかDicyclohexylcarbodiimide(DCC)です。初めにDCCがカルボン酸のプロトンを引っこ抜き、カルボキシアニオンがDCCの炭素を求核攻撃します。ここで、ーOH基が無くなったため、アミンがカルボニル炭素に求核攻撃し、求核アシル置換が起きます。最後にカルボニル酸素上の電子がπ結合としてカルボニル二重結合を形成し、アミドと尿素系化合物を生成します。
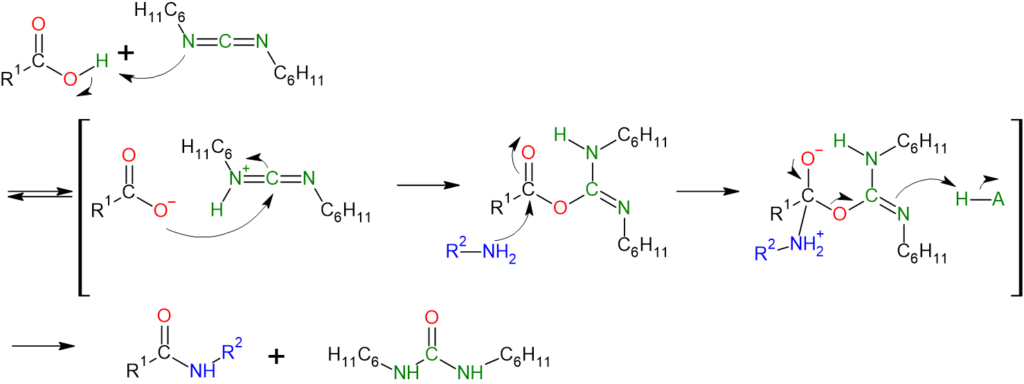
図7.DCCを用いたカルボン酸とアミンのアミド結合
ちなみに、DCCを用いると二つのアミノ酸をアミド(ペプチド)結合させ、ジペプチドを形成することができます。
関連記事(ペプチド、タンパク質)

カルボン酸の酸塩化物化
他にもカルボン酸と塩化チオニル(チオニルクロライド)と反応させることで、酸塩化物を生成することができます。この反応は求核アシル置換経路によって起こり、カルボン酸がまずアシルクロロ亜硫酸中間体に変換され、ーOH基がより優れた脱離基に変換されます。その後、塩化物イオンに求核攻撃され、酸塩化物が生成されます。この反応はHCl、SO2といった強酸が発生するため、酸抑制剤として第三級アミンを加える必要があります。
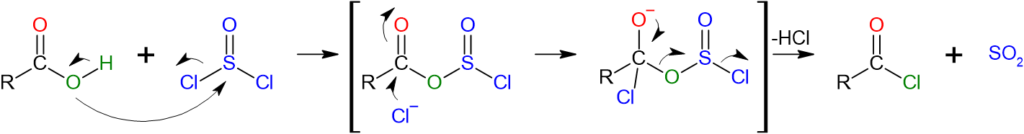
図8.塩化チオニル(チオニルクロライド)を用いたカルボン酸の酸塩化物化
ちなみに、酸臭化リンPBr3を用いると、酸臭化物ーCOBrを合成することができます。
酸ハロゲン化物の反応
酸塩化物、酸臭化物といった酸ハロゲン化物は良好な反応を示します。これらは水、カルボキシアニオン、アルコール、アミン、およびGilman試薬と反応させることで、カルボン酸、酸無水物、エステル、アミド、およびケトンを生成することができます。逆に言うと、水と反応させてしまうとカルボン酸に戻ってしまうため、水には触れさせてはいけません(Grignard試薬よりはマシですが…)。
また、強酸であるため、取り扱いは要注意です。間違っても強アルカリを近くに置いてはいけません。うっかり冷却せずに混ぜてしまうと、一気に発熱反応が起こり大変危険です。
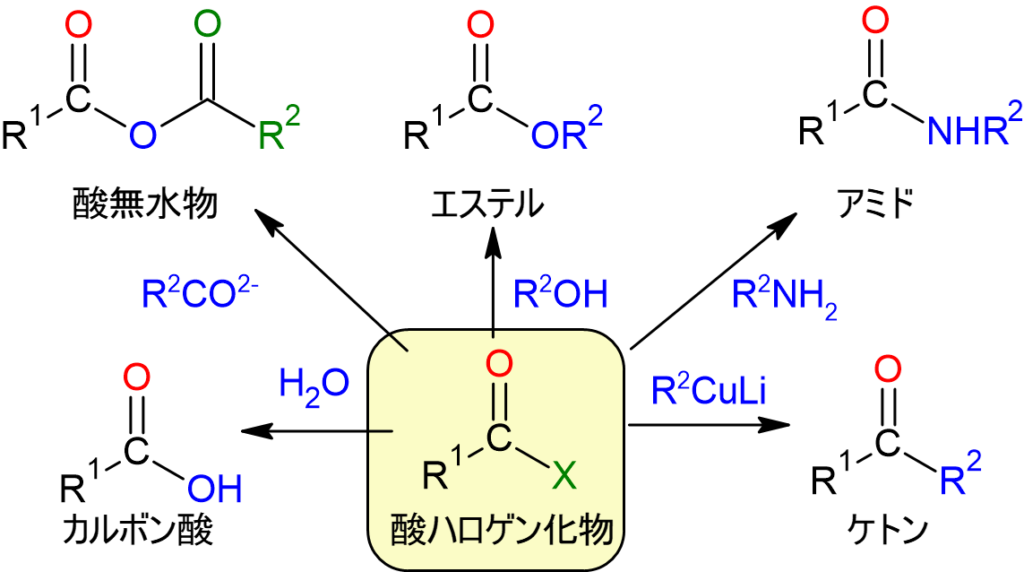
図9.酸ハロゲン化物の反応例
Gilman試薬以外の反応機構としては基本的には酸素O(アミンの場合は窒素N)上の非共有電子対がカルボニル炭素Cに求核攻撃をし、塩化物イオンが脱離します。その後、塩基(第三級アミン)を用いてプロトンを引っこ抜き、各生成物ができあがります。代表として、アルコールの反応機構を下図に示します。
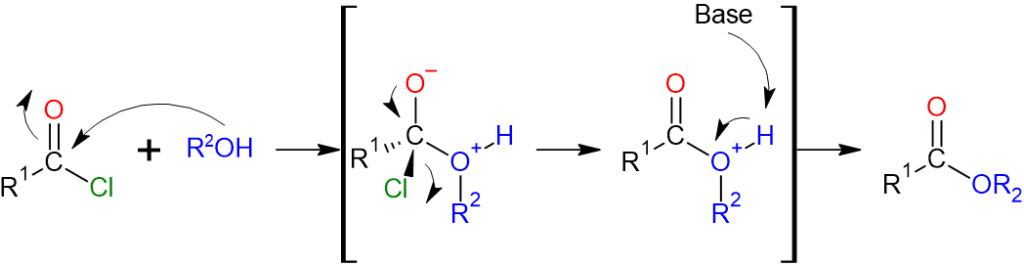
図10.酸ハロゲン化物の反応機構
ちなみに、上記でFischerエステル化、DCCを用いたアミド化を紹介しましたが、基本的には酸ハロゲン化物にしてからエステル、アミド化にする方が高収率で一般的です。もちろん、酸ハロゲン化物は強酸なので取り扱い要注意ですが。
最後に、Gilman試薬を用いたケトンの生成を解説します。エーテル溶媒中、反応にもよりますが、約ー80℃とかなり低温条件下でリチウムジオルガノクプラート(Li+R22Cu–)による求核攻撃から反応が始まり、アシルジオルガノクプラート中間体を経て、R2Cuが脱離されてケトンが生成されます。
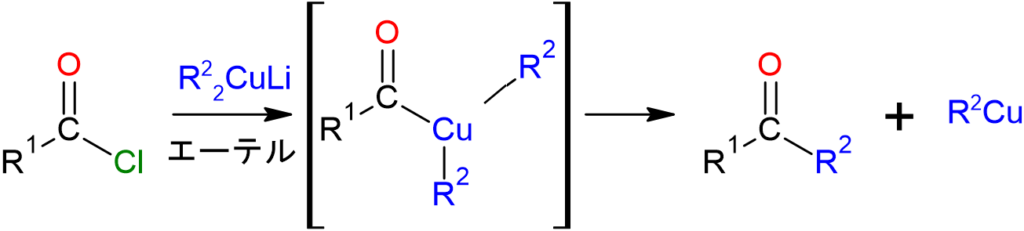
図11.Gilman試薬を用いたケトンの生成
以上が酸ハロゲン化物を用いた反応です。基本的にはカルボン酸では反応が起こりにくいため、一度酸ハロゲン化物にしてから反応するのが理想です。しかし、危険な強酸となる、刺激臭、反応性が高いため、反応にもよりますが、酸抑制剤(基本的には第三級アミン)を含みながら添加時は冷やしながらゆっくりと加える必要があります(Gilman試薬はさすがに冷やし過ぎですが…)。
ちなみに、反応性はアミド<エステル<チオエステル<酸無水物<酸ハロゲン化物です。つまり、反応をしたければ酸ハロゲン化物にすることが理想ですが、逆にいうとアミドは安定な結合ともいえます。基本的にはアミド結合は強アルカリ水溶液中での加水分解しか結合が切れません。
まとめ
・カルボニル化合物はカルボニル基C=Oが存在する化合物の総称
・カルボニル基はCδ+、Oδ-に分極しており、炭素は求核攻撃されやすく、酸素は求核攻撃をしやすい
・カルボニル基はGrignard試薬や還元剤LiAlH4、NaBH4(LiAlH4の方が還元力は強いが、危険)を用いて還元することが可能、Grignard試薬は置換基を導入、還元剤は水素還元
・カルボン酸は強酸を用いてアルコールとエステル化(Fischerエステル化)
・カルボン酸はDCCを用いてアミンとアミド化
・酸ハロゲン化物が最も反応性良好(上述の反応よりエステル化、アミド化しやすい)、強酸なため、取り扱い要注意、反応には酸が発生するため、第三級アミンが必要
・反応性は(安定)アミド<エステル<チオエステル<酸無水物<酸ハロゲン化物(反応性大)
以上が、カルボニル化合物の反応例ですが、ここでは説明しきれていない反応もあります。以下の参考文献ではもっと詳しく記載されています。
参考文献「マクマリー有機化学(中)」J. McMurry 著
本日はここまで!! 最後まで読んで頂きありがとうございました!!

コメント