こんにちは。 ミドリケムです。
本日はコロイドの電気的性質について解説していきます。
コロイドを含め、界面には電荷の隔たり、つまり電気二重層が形成されます。
「電気二重層って何?」
「界面で何が起きているのかイメージできない…」
この記事では、
・界面電気化学の基本
・コロイドとの関係(凝析、塩析、親水コロイド)
・電気二重層(ζ(ゼータ)電位)の仕組み
を図とイメージでわかりやすく解説します。
コロイドの基本的性質は以下の記事で解説しています。

結論から言うと、界面では電荷が分離し、「電気二重層」が形成されています。この構造が、コロイドの安定性や電気化学反応を支配しています。どういうことなのか、順を追って解説していきます。
コロイド溶液の安定性について
コロイド粒子がは10-9~10-6m程度のサイズです。ではなぜ沈殿しないのか疑問に思ったりしましたか?沈殿しない理由は以下の3つです。
1.ブラウン運動
2.コロイド粒子の電気的反発
3.コロイド粒子の表面と溶媒との相互作用
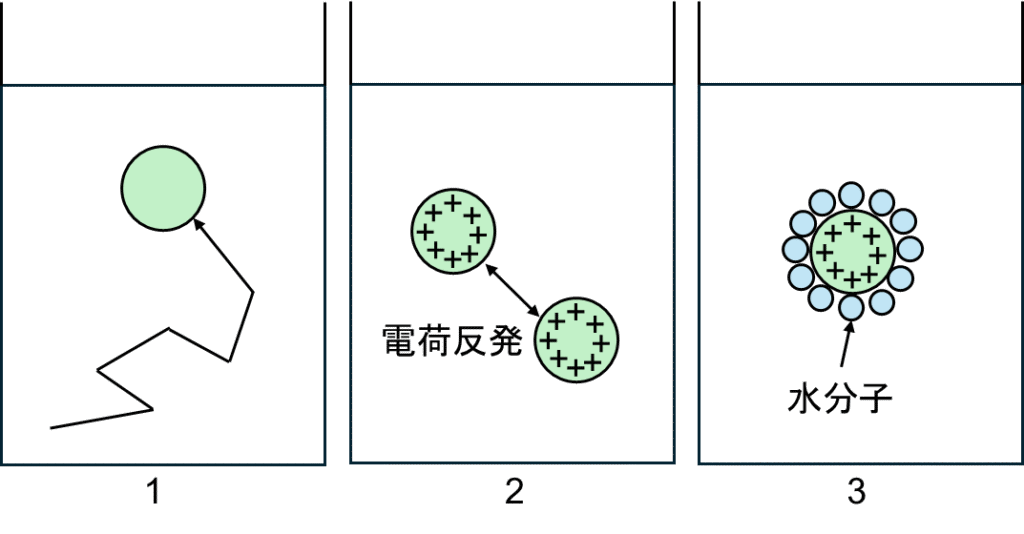
図1.コロイドが分散している模式図
2.3.に関しては電気的性質が関わっていますね。コロイドも表面にイオンが存在すると、電荷を帯びます。
逆をいえば、この電荷反発や溶媒和が無くなるとコロイドは沈殿します。それについて解説していきます。
コロイドの沈殿
凝析とは?
電気的反発しているコロイド粒子を沈殿させてみましょう。
例として、水酸化鉄(Ⅲ)(化学式はFe(OH)3であるが、不安定なため実際は酸化水酸化鉄FeO(OH)であることが多い)のコロイド溶液(分散媒は水)を沈殿させることにしましょう。
水酸化鉄(Ⅲ)は水に不溶なため、電離しません。しかし、コロイド粒子並に小さくなり、見かけ上は赤褐色の水溶液の様です。
このように、水和されにくいコロイドのことを疎水コロイドといいます。
水酸化鉄(Ⅲ)は-OH基はむき出しになっているため、ここに未反応のFe3+やH+がくっつきます。つまり、表面は正電荷です。そのため、電荷反発によりコロイド粒子として存在しています。
そのコロイド溶液に電解質として硫酸ナトリウム水溶液Na2SO4aqを少量加えると、硫酸イオンSO42-がコロイド粒子同士の仲介となり電荷反発が抑えられ、コロイド粒子同士が凝集して沈殿します。図示すると、以下の通りです。
凝集して析出したため、この現象を凝析といいます。
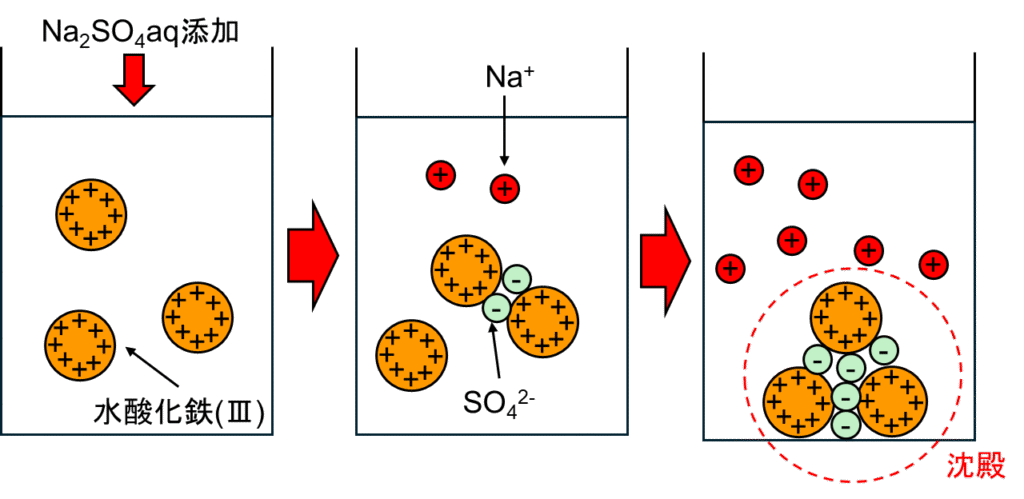
図2.コロイドが沈殿する(凝析)模式図
塩析とは?
次に、溶媒と相互作用しているコロイド粒子を沈殿させてみましょう。
水と水和しているコロイド、すなわち親水コロイドはイオンの様に水分子と相互作用しているため、沈殿しません。それでは水和した水分子を剝がしましょう。
親水コロイドにも硫酸ナトリウム水溶液Na2SO4aqを加えると、電解質がコロイドから水分子を引き剝がします。その後は凝析と同様、対となるイオンにより沈殿します。そのため、疎水コロイドよりは電解質が多量に必要としています。図示すると、以下の通りです。
分散媒分子を一度引き剥がした後に凝析する現象を塩析といいます。
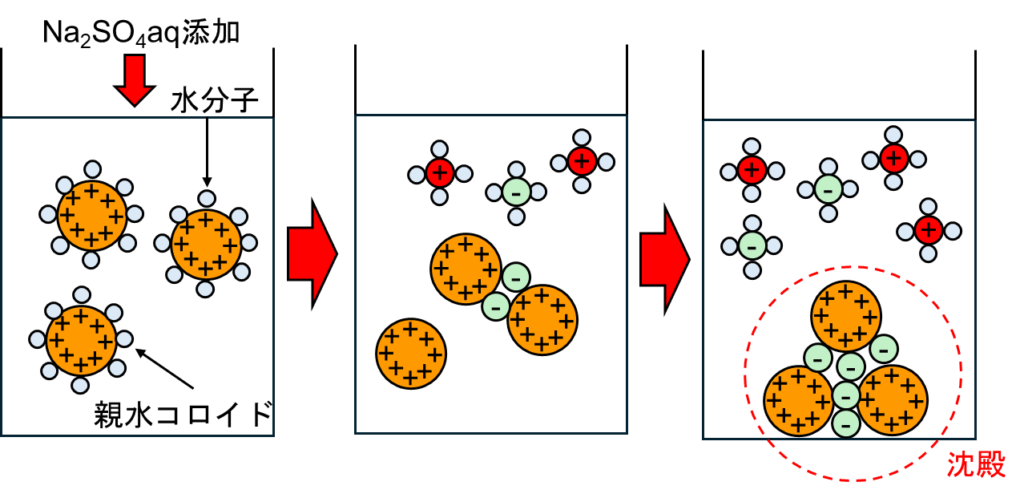
図3.コロイドから水分子を剥がし、沈殿する(塩析)模式図
この様に、親水コロイドは疎水コロイドより沈殿しにくいです。逆に言うと、疎水コロイドの表面を親水コロイドで覆いかぶせることで安定して分散させることができます。この親水コロイドのことを保護コロイドといいます。
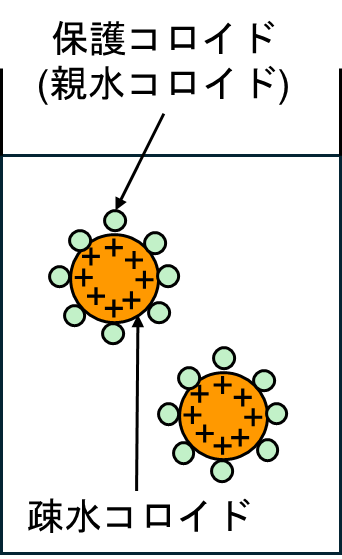
図4.保護コロイドの模式図
電気二重層とは?
先程のコロイドの図は簡単に描きましたが、コロイド表面について、もう少し詳しく解説します。上の図ではコロイド表面の電荷は簡単に描きましたが、実際は電気二重層が形成されています。
なぜ電気二重層ができるのか?
→ コロイド表面は電荷を持つ
→ 溶液中のイオンはそれに引き寄せられる
その結果、界面で電荷が分離する。
詳しく解説していきます。
コロイド粒子の表面は帯電しており、その周囲には反対符号のイオンが集まります。粒子のすぐ近くには強く引き寄せられたイオンの層(固定層)ができ、その外側にはイオンがゆるやかに拡散する層(拡散層)が存在します。
この時にできた二重の層を電気二重層といいます。
粒子が水中で移動するとき、固定層が一部の水分子とともに動きます。このとき実際に粒子と共に運動する境界面を「すべり面」と呼び、その面での電位をζ(ゼータ)電位といいます。
イメージで例えると、コロイドは固定層というコートを着ており、当然、コロイドが動くと固定層というコートも一緒に動きます。また、その時のコートの外側の表面(すべり面)の電位がζ電位です。
文章では中々理解しにくいため、図示します。コロイド表面は電荷を帯び、その付近には反対の符合のイオンが集まります。今回はコロイド表面を正とします。すると、溶液側には負電荷イオンが集まります。この層を電気二重層といいます。
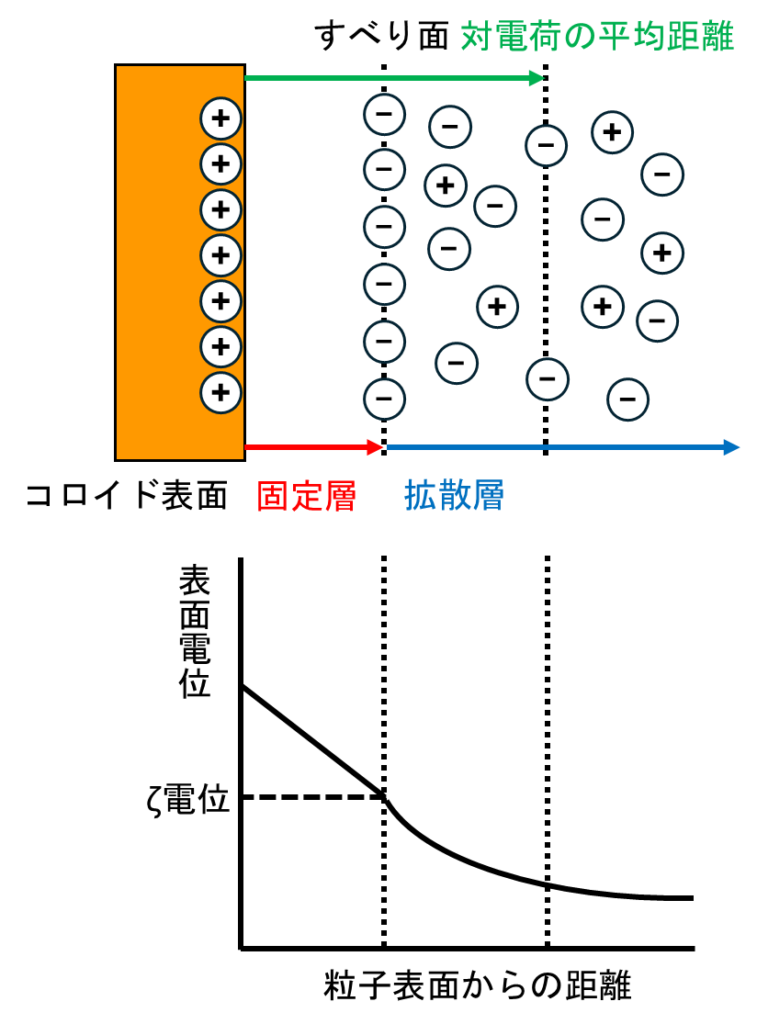
図5.電気二重層の模式図と表面からの距離と電位との相関グラフ
コロイド表面ー固定層ーすべり面(ζ電位)ー拡散層という順で並んでいます。
固定層までは電荷は直線的に低下していきますが、固定層(ζ電位)以降は指数関数の様に低下していきます。
ちなみに、測定でわかるのはζ電位のみです。
また、今回はコロイド粒子のことについて解説しましたが、このような界面構造は、電池や触媒の性能にも大きく影響します。
関連記事↓↓



まとめ
・疎水コロイドを析出させる方法は凝析(電解質は少量)
・親水コロイドを析出させる方法は塩析(電解質は多量)
・保護コロイド…疎水コロイドを保護する役割をもつコロイド
・界面では電荷が分離する
・その結果、電気二重層が形成される
・コロイドの安定性はこの構造に依存する
以上がコロイドの簡単な解説です。次回は界面活性剤について解説しようかと思います。

参考文献「入門コロイドと界面の科学」近藤 保、鈴木四朗 著
本日のブログはここまで。 最後まで読んで頂きありがとうございました。



コメント