こんにちは⭐ ミドリケムです。
本日は酸・塩基について解説していこうかと思います。
皆さん酸・塩基って覚えていますか?中には塩基って何!?アルカリじゃないの!?と思われた方もいらっしゃると思います。
今後、皆さんの身近にあるタンパク質(プロテイン)の事や洗剤の事についても解説していきたいのですが、やはりそれにはこの様な基本的な事からおさらいする必要があります。
タンパク質や洗剤の関連記事


酸・塩基の定義って覚えていますか?定義は大きくわけて3つあります。アレニウスの定義、ブレンステット・ローリーの定義、ルイスの定義です。他にもルックス・フロッドの定義等あるみたいですが、重要なのはこの3つの定義です。順を追って説明します。
1.アレニウスの定義とは?
これが一番有名な話ですね。中学の理科でも学習します。簡単に言うと、水中に溶かすと電離(電荷的に分離という意味)し水素イオン、つまりプロトンH+を放出する物質が酸、水酸化物イオンOH–を放出する物質が塩基です。そして、これを数値としてわかりやすくしたものがpH(ピーエイチ、もしくはペーハー)です。pは簡単にいうとマイナス常用対数という意味です。水素イオン濃度を[H+](mol/L)と表すと以下の式の通りとなります。
pH=-log10[H+]
つまり、pHは水中での水素イオン濃度を示しています(厳密には水中で水素イオンと水がくっついたヒドロにウムイオン、H++H2O→H3O+)。
ちなみに今回はご丁寧に対数の底を10と記しましたが、科学の世界では省略して書くことが多いです。自然対数と並べて数学の世界と書き方が違ってきます。詳しくは以下の表の通りです。
| 底 | 表記(科学の世界) | 表記(数学の世界) | |
| 常用対数 | 10 | logx | log10x |
| 自然対数 | ネイピア数e=2.718.. | lnx | logx |
なぜ違うんだろう… といつも疑問に感じます笑。
気を取り直してpH=7が中性([H+]=10-7mol/L)、それ以下なら酸(pH=2だと[H+]=10-2mol/L)、それ以上だと塩基(pH=13だと[H+]=10-13mol/L)となります。
逆に水中での水酸化物イオンの濃度、あまりメジャーではありませんがpOHは以下の様に示します。
pOH=14-pH=-log10[OH–]
pOHはpOH=7だと中性、それ以下なら塩基、それ以上なら酸となります。かなりマイナーなので参考までに。
酸で有名なのは塩酸HCl、硝酸HNO3、硫酸H2SO4、酢酸CH3COOHであり、塩基で有名なのはNaOH、KOH等ですね。
え、アンモニアは塩基ではないの!?と疑問に思った方。確かにアンモニアは水に溶けると水酸化物イオンを生成し、水溶液は塩基性を示します。式としては以下の通り。
NH3+H2O→NH4++OH– 参考:NaOH→Na++OH–
水酸化ナトリウムは水に溶かすと水酸化物イオンを放出するので塩基ですが、アンモニアからは水酸化物イオンを放出していないのでアレニウスの定義では塩基とは言えないのです。でも水溶液は塩基性を示すから納得がいかない!!っと思ったそこのあなた。そこで次の定義が登場するのです。
2.ブレンステッド・ローリーの定義
これは高校化学から登場します。個人的にはこれが化学技術者にとって最も一般的ですね。酸・塩基の定義といえばパッと思いつくのはこの定義です。結論から言うと、水素イオンH+を放出する物質が酸、逆に受け取る物質が塩基です。
さっきのアンモニアを例にとってみましょう。アンモニアNH3は水素イオンH+を受け取りアンモニウムイオンNH4+になったため塩基、逆に水は水素イオンH+を放出したため酸という訳です。
水が酸?と中々しっくりきませんよね。かくいう私も高校生時代しっくりきませんでした。もっというと、アレニウスの定義は水中に溶かす事が前提でしたが、ブレンステッド・ローリーの定義では水中に溶かすことは前提ではありません。定義にも「水中」という言葉は出てきていませんよね。
ちなみに、アレニウスの定義での酸はすべて水素イオンを放出しているため、ブレンステッド・ローリーの定義でも酸、アレニウスの定義での塩基は水酸化物イオンを放出し、それが水素イオンを受け取って水分子を形成するため、ブレンステッド・ローリーの定義でも塩基となります。つまり、アレニウスの定義を拡張したのがブレンステッド・ローリーの定義です。ベン図で描くと以下の通りです。
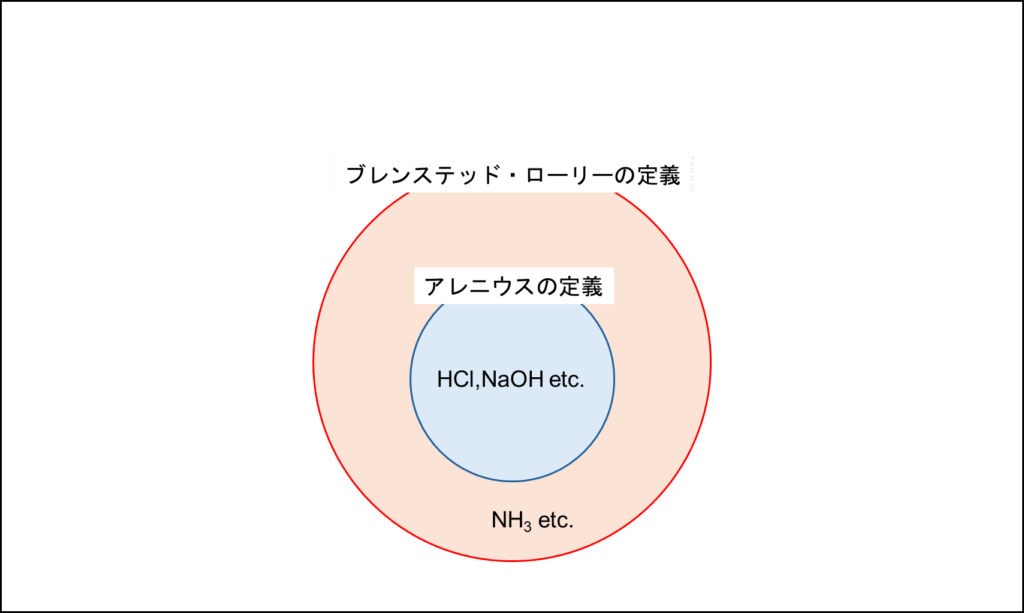
図1.酸・塩基の定義①
ちょっとわかりやすくなりましたかね?
ここで、「アルカリ(alkali)」と「塩基(base)」の違いです。アルカリはアラビア語で「植物の灰」という意味です。植物を燃やすことにより発生する水酸化物を指していました。つまり、アレニウスの定義の塩基のみ別名「アルカリ」と呼びます。そのため、「アルカリ」と「塩基」の違いと言いましたが正しくは「アルカリ」は「塩基」の一部です。
中学まではアレニウスの定義のみ学習したため「アルカリ」と呼んでいましたが、高校からブレンステッド・ローリーの定義まで広がったため「塩基」と呼ぶことになったのです。
ちなみに、先程のベン図にはまだ空白が多いことに気が付きましたか? そうです。まだ定義は広がるのです。
3.ルイスの定義
これは大学化学から登場します。そのため、知らない人も多いかと思います。結論としては、非共有(孤立)電子対を受け取る物質が酸、提供する物質を塩基と呼びます。先程のアンモニアと水の反応を例にとってみましょう。水分子中の水素原子はアンモニア分子中の窒素上の非共有電子対を受け取っています。図示するとこんか感じです。
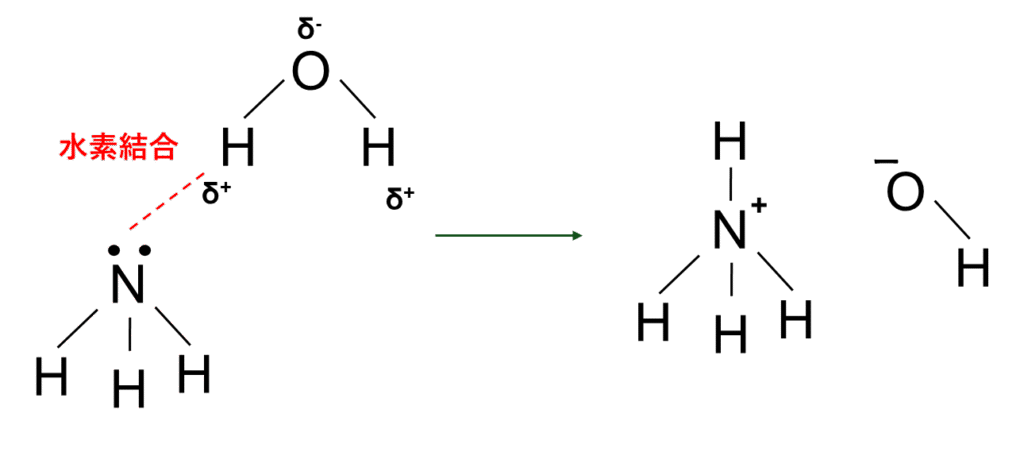
図2.水分子間の相互作用(水素結合)
水分子の水素は+に分極、つまりちょっと+になっています(これがδ+)。逆にアンモニア分子中の窒素は非共有電子対を持っているため、ーの電荷が強いです。それがアンモニアの非共有電子対と水素結合という相互作用へと結びつき、やがて、水分子から水素を奪い取ります。言い換えると、水分子中の水素は非共有電子対を受け取り、アンモニア分子中の窒素は非共有電子対を提供します。
関連記事↓↓

よって、水はルイス酸、アンモニアはルイス塩基となります。もっと言うと、水素イオンはルイス酸、水素イオンを受け取る塩基はルイス塩基と呼び、さらに定義が拡張します。ベン図でいうとこんな感じです。
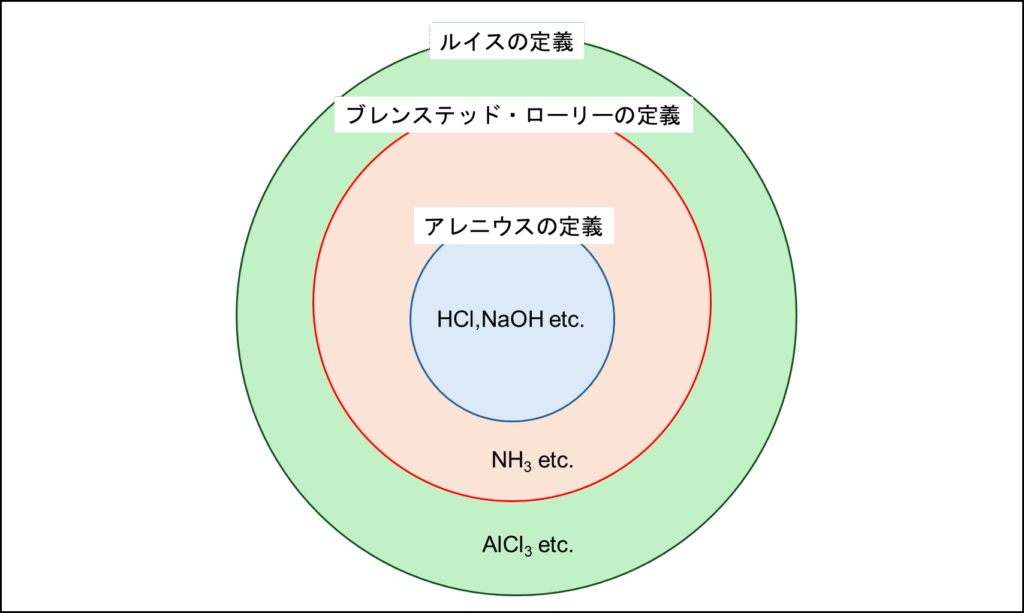
図3.酸・塩基の定義②
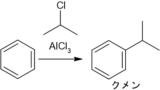
ここでアレニウス、ブレンステッド・ローリーの定義にはないルイス酸として塩化アルミニウムAlCl3が登場しました。塩化アルミニウム上のアルミニウムAlには非共有電子対を受け取る場所があり、これが酸無水物や酸クロライド等から電子対を受け取り、カチオン(正電荷を持った物質)として、ベンゼン等の芳香族が求電子置換反応を起こします。これをフリーデル・クラフツ(Friedel-Crafts)反応と呼びます。
ちょっと難しい内容なので詳細は割愛しますが、要は酸は水素イオンH+以外にもあるという事になります。
関連記事(フリーデル・クラフツ(Friedel-Crafts)反応)
以上が酸・塩基の説明となりました。ちょっと難しかったですか? 冒頭にもお伝えした通りこのブログでは身近な化学の事について解説していこうかと思っていますが、どうしても基礎的な内容はおさらいしておかないといけないと思いこの様なブログを発信しました。少しでも酸・塩基の事を思い出したり理解してくれたりしてくれたら幸いです。
また、酸・塩基はHSAB則もあり、詳しくは以下の記事で解説しています。
関連記事(HSAB則)

本日はここまで。最後まで読んで頂きありがとうございました。



コメント