こんにちは⭐ ミドリケムです。本日は結合について解説していきます。
皆さん原子、分子はどうやって結合していると思いますか?主に5つご紹介します。
・共有結合(配位結合)
・イオン結合
・金属結合
・水素結合
・ファンデルワールス結合
なんか昔化学でやったことあるなー、ぐらいのイメージかもしれません。また、現在高校生や、社会人で高校化学の勉強をし直している方々はこれらの違いがよくわからない、説明してほしい💦と思っているかもしれません。本日はこれらを説明していきます。
共有結合とは?
まずは共有結合です。これは次に説明するイオン結合とごっちゃになっている人も多いかと思います。
以前のブログで原子は周期表の一番右にある18族、つまり貴ガスになりたがると説明した事を覚えていますか?貴ガスは電子が入っている部屋、つまり電子殻に電子が過不足なくすっぽり入っているため、かなり安定化しているのです。
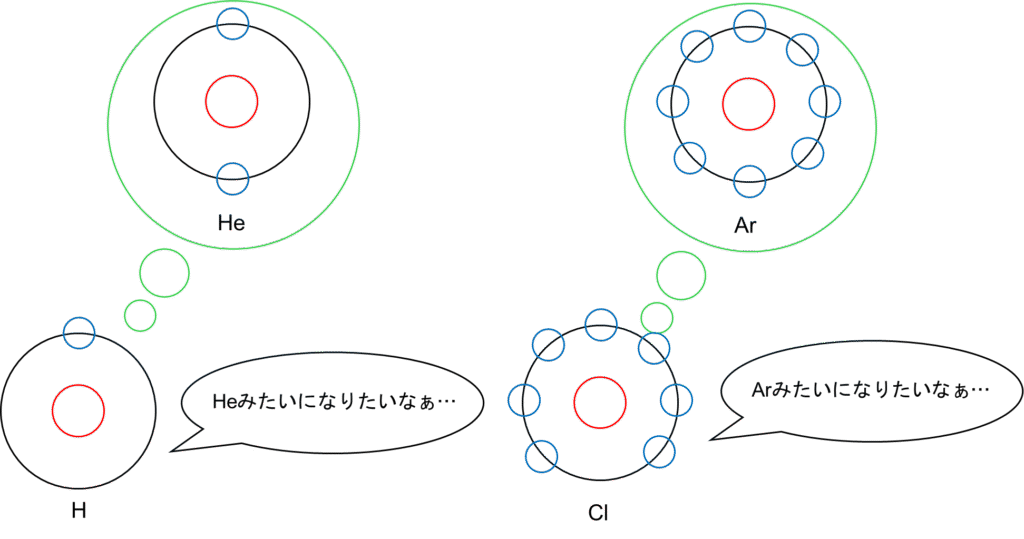
主に水素はヘリウムに、ナトリウムはネオンに、塩素はアルゴンに、といった形です。
しかし、水素、塩素からしたら電子が1個足りない💦ナトリウムからしたら電子が1つ多い💦となってしまいます。それを解消するのが共有結合、あるいは次項で説明するイオン結合です。
塩化水素を例に説明します。塩化水素って覚えていますか?塩酸に溶解している物質HClですよ。というか、塩酸は塩化水素が水に溶けた溶液、つまり、塩化水素水溶液と思った方がいいですね。塩酸の別名は塩化水素酸ですし。
水素、塩素はどちらも貴ガス構造になるためには電子が1つ足りないといいましたね。ではお互い電子を1個ずつ分け与えて貴ガス構造になろうぜ♪っという感じですね。まとめると、以下の様な図になります。
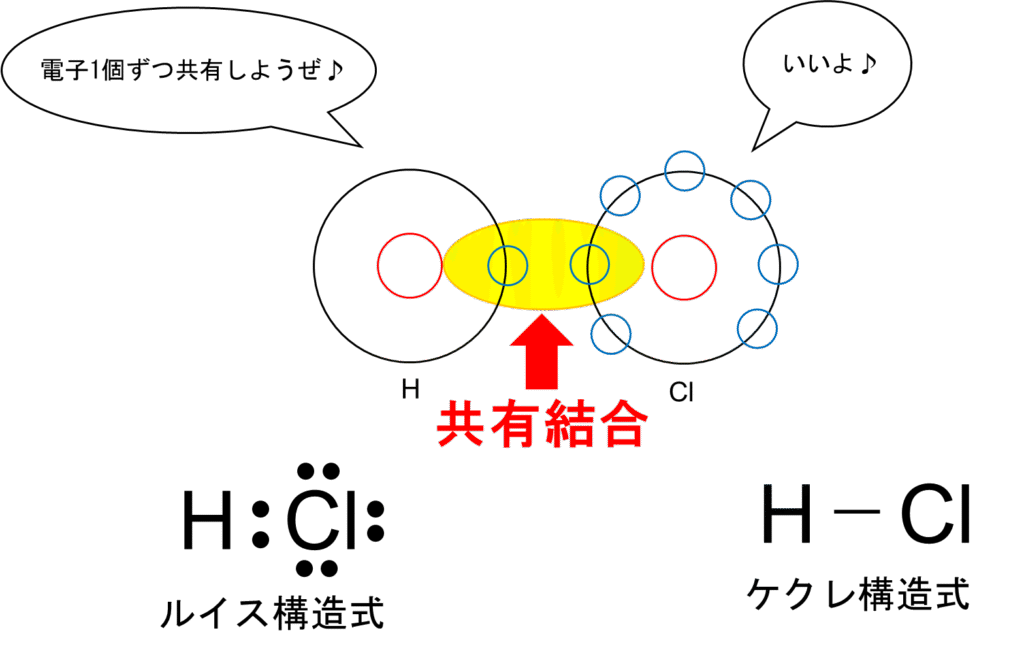
この様に電子を1個ずつ共有し合ってできた結合を共有結合といい、この時にできた電子対を共有電子対といいます。構造式はルイス構造式とケクレ構造式があり、ルイス構造式は電子を点で表した式、ケクレ構造式は電子対のみを線で表した構造式です。
電子対は何も1本とは限りません。酸素分子は2本O=O、窒素分子は3本N≡Nと表します。これらを単結合、二重結合、三重結合といいます。
また、結合を形成する二つの原子の一方のみから結合電子2つが提供され、共有結合として形成される場合もあります。これを配位結合といいます。配位結合は共有結合の一部と思って下さい。
イオン結合とは?
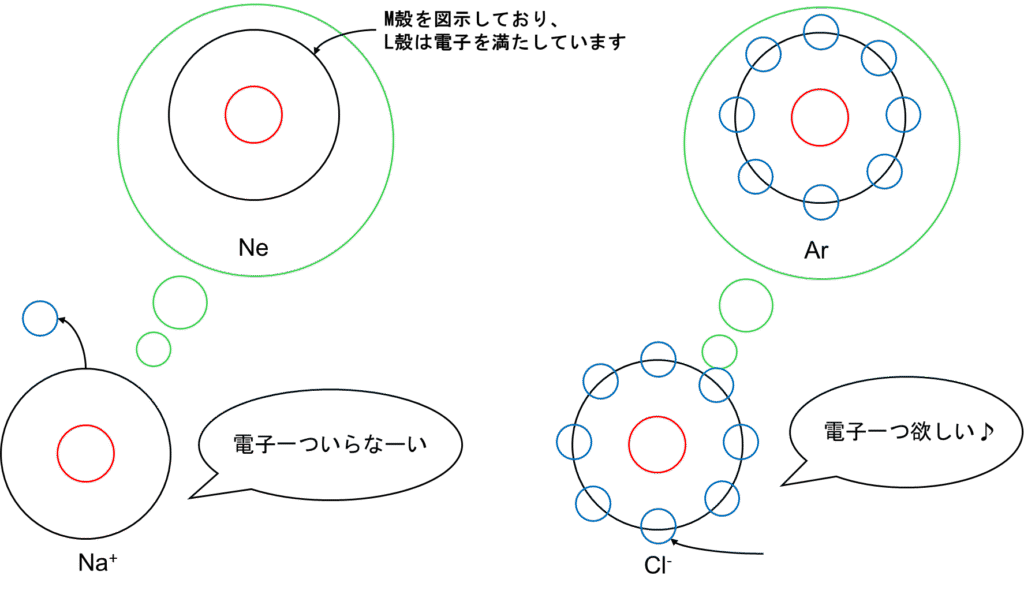
次にイオン結合です。代表例としては塩化ナトリウムNaClです。塩化水素HClは電子を共有し合ってお互いに貴ガス構造になっています。ところが、塩化ナトリウムはナトリウムはネオン型になりたがっているため、電子が一つ余分です。逆に塩素はアルゴンになりたがっているため、電子が一つ欲しがっています。つまり、ナトリウムが電子(マイナス電荷)一つ失ったナトリウムイオンNa+と塩素が電子(マイナス電荷)一つ多く持った塩化物イオンCl–が静電気力(クーロン力)により磁石のようにくっつきます。図にすると以下のような感じです。
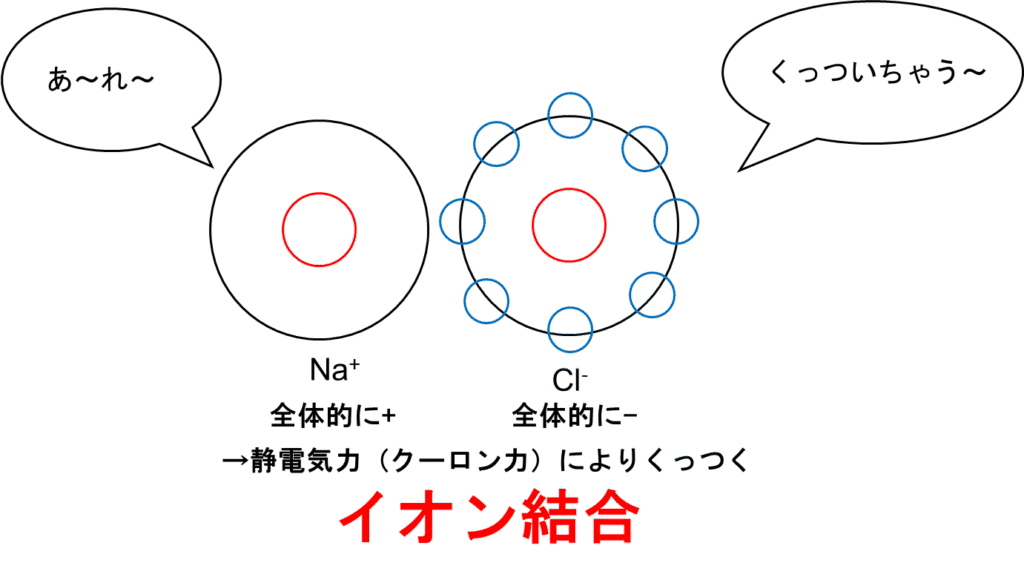
これをイオン結合といいます。
ここで、共有結合とイオン結合の違いを詳しく説明します。
その前に電気陰性度について説明します。電気陰性度とは原子が電子を引き付ける力を示したものであり、数値が大きい程電子を引き付けます。
主にポーリングの定義によって決められた値として、水素Hは2.20、ナトリウムNaは0.93、塩素Clは3.16です。並べると、Na<H<Clです。
つまり、塩素が水素、ナトリウムの電子を引っ張っています。水素は多少電子を引っ張り返すことができるのですが、ナトリウムは完全に電子を奪われてしまいます。
つまり、共有結合は電子の偏りは多少あるかもしれませんが、二つの電子対は水素の物でもあり塩素の物でもあります。一方、イオン結合は完全に電子がナトリウムから塩素に奪われてしまい、静電気力によりくっついた状態です。
主に1族(アルカリ金属),2族(アルカリ土類金属)は電子を放出し、逆に16族、17族(ハロゲン)は電子を受け取りやすくなります。つまり、前者は電気陰性度が低く、後者は電気陰性度が高いというわけです。これにより結合の種類が変わってきます。
金属結合とは?
3つ目は金属結合です。金属結合とはその名の通り、主に金属同士の結合です。原子は原子核(陽子+中性子)の周りに電子が飛び回っていると言いましたね。金属はその電子が金属原子核が規則正しく配列し、その周りを電子が自由に飛び回っているのです。この時の電子を自由電子と呼びます。図示すると以下の感じです。
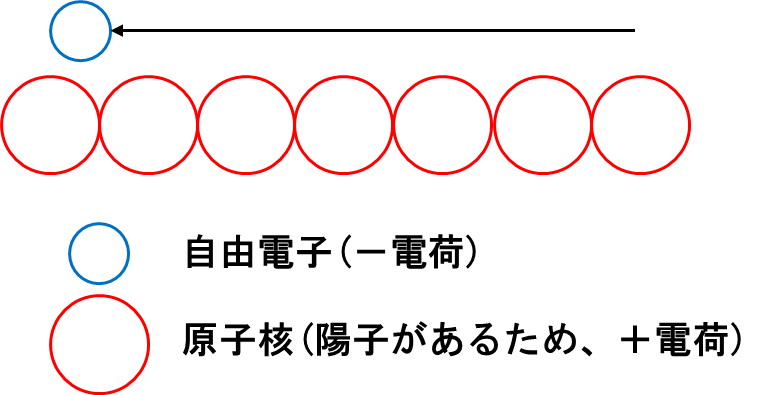
イメージとしては原子核という海の中に自由電子が自由に飛び回っているのです。自由電子や原子核との間に相互作用が働くため、金属原子同士が結合します。これが金属結合です。
そして、電圧がかかると自由電子は規則正しく直進するのです。そのため、金属は電流が流れます。また、金属特融の光沢も自由電子が影響しています。
水素結合とは?
水素結合とは電気陰性度により電子が少し不足した水素が非共有電子対(孤立電子対)を持った原子、主に酸素O、窒素N、フッ素Fと弱い相互作用によりくっつく結合です。水分子で示すと以下の図示の通りです。

ここで、δ+、δ–とちょっと難しい記号が出てきましたが、要はちょっと+、ちょっとーというイメージで結構です。このように水分子同士は水素結合により分子同士がくっついています。このまま、酸素原子が水素原子を引っこ抜きヒドロにウムイオンH3O+になったりします。式で表すと以下の通りです。
2H2O→H3O++OH–
ヒドロにウムイオンは他の水分子、もしくは水酸化物イオンに水素を奪われたりします。まとめると水分子は酸素原子による水素原子の取り合いです。そのため、水はH2Oと小さい分子にも関わらず液体として存在するのです(本来は気体としか存在できません)。
ファンデルワールス力結合とは?
ファンデルワールス結合とはファンデルワールス力により分子同士が結合した非常に弱い結合です。そのまんまですね💦
これを聞くとファンデルワールス力って何?と思いますよね?難しく言うと、双極子モーメントや分極の誘導や配向あるいはロンドン分散力により…
いやいや、もうわからん💦となりますね笑 要は物理吸着です。水で濡れたガラス板同士がくっつくみたいな感じです。これを説明すると先程の様なかなり難しい事を語らなければならないため、ここでは割愛します。
以上が結合です。結合の強い順番としては共有(配位)結合>イオン結合>金属結合>水素結合>ファンデルワールス結合です。原子の種類にもよりますが。
世の中の物質は主にこれらの結合により成り立っており、化学の世界でもこれらを理解しておく事はとても重要になります。少し難しかったかな?しかし、基本事項としてしっかりと理解しておきましょう。
本日はここまで。最後まで読んで頂きありがとうございました!!



コメント