こんにちは。ミドリケムです。今回は原子について解説していこうかと思います。
皆さん高校化学の内容を覚えていますか?もしかしたら履修していない人もいるかもしれません。 そのため、今回は簡単な化学の基礎から学んでいこうかと思います。
世の中にある生物、物質含め、何からできていると思いますか?そう、「原子」です。よく「元素」とごっちゃになっていると思いますが、簡単に違いを説明するとこんな感じです。
原子…物質を構成する最小単位
元素…特性、性質の違いを表すもの
自分でも説明するのは難しいのですが、要は物質を構成するものを「原子」、性質を表すものを「元素」というイメージで良いと思います。
そして、原子は主に「陽子」「中性子」「電子」の3つの粒子から構成されています。そして、「陽子」はプラス、「電子」はマイナスの電荷を帯びており、「中性子」は電荷を帯びていません。そして、「陽子」「中性子」をまとめたのを「原子核」と呼び、原子核の周りに電子が飛び交っています。これが原子となります。図に説明するとこんな感じです。
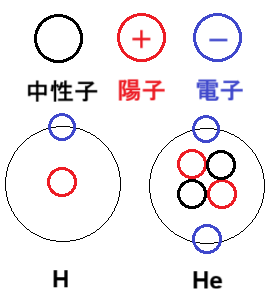
図1.水素HとヘリウムHeの原子模式図
水素Hは陽子、電子それぞれ1つずつあるので電荷的に中和されます。ヘリウムHeも陽子、電子2つずつあり、中性子は電荷を帯びないので電荷的に中和されます。そして、陽子の数=原子番号なのです。それをまとめたのが周期表です。
周期表の縦は「族」、横は「周期」といいます。1族がアルカリ金属、2族がアルカリ土類金属、17族がハロゲン、18族が貴(希)ガスといいます。ちなみに貴ガスが最も安定しており、どの原子も貴ガスになりたがっていると思って下さい。
つまり、アルカリ金属は電子を1つ放出しやすく、逆にハロゲンは電子を受け取りやすくなります。電子の受け渡しにもエネルギーが関連してきます。それは。「イオン化エネルギー」「電子親和力」です。具体的に説明すると、以下の通りです。
イオン化エネルギー…電子1個を取り去るのに必要なエネルギー
電子親和力…電子1個を受け取る時に放出されるエネルギー
また、電子の過不足により電荷を帯びている原子をイオンといいます。特に電子が取り去って全体的に+の電荷を帯びている原子を陽イオン、逆に電子を受け取りーの電荷を帯びている原子を陰イオンと呼びます。
化学を語る上で原子やイオン、電子等は避けて通れない内容です。
じゃあその原子、イオンはどうやって結合しているの?となりますよね。それは以下の記事で解説しています。

本日はここまで!最後まで読んでいただきありがとうございました!!
P.S.周期表に記載されている原子番号113番「ニホニウム」Nhは理化学研究所が発見した、すなわち日本人が発見した元素です。だからニホニウムという名前なんですね。



コメント